如何选用高表达 TFR&CD98 皮质神经元助力 CNS 药物研发?
在中枢神经系统(CNS)药物研发的征途上,血脑屏障(BBB)始终是横亘在成功面前的第一道天堑。而皮质神经元作为药物作用的最终靶细胞,其质量与功能性表达,直接决定了体外模型的可信度与药物筛选的成败。
基于专业的iPSC技术平台,赛业生物正式推出——高表达TFR & CD98的皮质神经元(iPSC来源),为您的BBB靶点研究、药物递送筛选、神经疾病模型构建,提供更可靠的细胞工具。
靶点信息:为什么是TFR和CD98?
全称:Transferrin Receptor 1
基因:TFRC
表达分布:
在脑微血管内皮细胞、神经元、增殖细胞、红细胞前体中高表达,BBB内皮细胞上尤为丰富。
核心功能:
1、通过受体介导转胞吞(RMT)将结合铁的转铁蛋白从血液侧转运至脑实质侧;
2、维持神经元铁稳态,参与髓鞘形成、神经递质合成和线粒体功能;
3、BBB靶向的“黄金标准”:利用抗TFR1抗体修饰的纳米粒、脂质体或腺相关病毒(AAV),可实现高效、特异的跨BBB递送。
应用方向:
1、BBB靶点研究中的应用
1)受体介导转胞吞的典范:TFR是BBB上最成熟的内源性转运系统之一。转铁蛋白与TFR结合后,经网格蛋白包被小泡内化、跨细胞转运,最后在脑侧释放。这一机制被广泛用于大分子药物脑递送(如抗体、酶、基因治疗载体)的设计。
2)BBB靶向的经典标准:利用抗TFR抗体(如8D3、OX26)修饰的纳米粒、脂质体或腺相关病毒(AAV),可实现高效、特异的跨BBB递送。研究显示,抗TFR1抗体融合蛋白的脑摄取量可比非靶向对照提高10-50倍。
3)神经元铁稳态调节:在皮质神经元上,TFR1负责摄取铁,铁是酪氨酸羟化酶(多巴胺合成限速酶)、髓鞘碱性蛋白等关键分子的辅因子。TFR表达异常与帕金森病、阿尔茨海默病中的铁沉积和氧化应激密切相关。
2、药物筛选与测试
1)靶向递送抗体筛选:以TFR为靶点,筛选抗体-药物偶联物(ADC)、纳米粒或AAV衣壳变体的跨BBB效率。常用方法包括:在BBB共培养模型中测试荧光标记载体的跨膜转运率,或通过竞争性抑制实验验证靶向特异性。
2)药物-转帖蛋白偶联策略:将小分子药物或核酸药物与转铁蛋白化学偶联,利用内源性TFR转运途径实现脑靶向。筛选时需检测偶联物是否保留转铁蛋白与TFR的结合活性,以及偶联后药物的活性和稳定性。
3)神经疾病靶点验证:在帕金森病、阿尔茨海默病、亨廷顿病等神经退行性疾病模型中,TFR1表达常发生改变。利用高表达TFR的皮质神经元,可评估铁螯合剂或TFR靶向治疗药物对神经元铁稳态、氧化应激和细胞存活的影响。
4)毒性测试:检测候选药物是否会干扰TFR介导的铁摄取。铁是神经元线粒体呼吸链的关键辅因子,若药物抑制TFR功能,可能导致线粒体功能障碍和神经元凋亡,是CNS药物早期安全性评价的重要指标之一。
基因:SLC3A2
表达分布:在脑微血管内皮细胞、神经元、肿瘤细胞、活化淋巴细胞等多种细胞中均有高表达。
核心功能:
1、调控L型氨基酸(如亮氨酸、苯丙氨酸)的跨膜转运;
2、参与整合素信号通路,调节细胞黏附、迁移和增殖;
3、在BBB中,参与维持屏障完整性及营养物质转运。
应用方向:
1、BBB靶点研究中的应用
1)屏障功能维持:CD98在脑微血管内皮细胞上高表达,与整合素β1结合,调控紧密连接蛋白(如Claudin-5、Occludin)的定位与表达,从而维持血脑屏障的完整性。
2)氨基酸转运枢纽:CD98/LAT1复合物是大分子中性氨基酸(如L-DOPA、甲状腺激素、某些药物前体)穿越BBB的主要通道。这一转运系统为前药设计提供了经典靶点。
3)神经元代谢支持:在皮质神经元上,CD98负责摄取必需氨基酸,支持神经递质合成(如谷氨酸、GABA的前体)和神经元存活,是神经元-内皮细胞代谢偶联的关键节点。
2、药物筛选和测试
1)药物设计和筛选:利用CD98/LAT1的底物特性,将药物与氨基酸(如L-苯丙氨酸)偶联,设计能主动穿越BBB的前药。通过检测药物竞争性抑制L-亮氨酸摄取的IC50值,筛选高亲和力候选分子。
2)神经元靶向验证:在皮质神经元-内皮共培养模型中,通过敲低或过表达CD98,评估候选药物进入神经元的能力,区分载体介导转运与被动扩散。
3)神经毒性测试:检测药物是否干扰CD98介导的氨基酸转运,若药物抑制CD98功能,可能导致神经元因必需氨基酸缺乏而出现代谢毒性,这是早期神经毒性筛选的重要指标之一。
产品名称:iPSC来源皮质神经元
服务编号:SY-iCN-00001
供应形式:冻存细胞(1×10^6)
流式检测验证:
赛业生物皮质神经元流式检测结果如下:
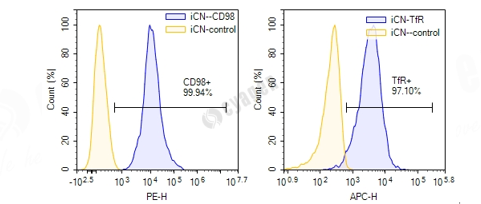
| 检测靶点 | 阳性率 |
|
TFR(CD71) |
97.10% |
| CD98 | 99.94% |
这意味着:
- 高纯度
近乎100%的神经元表达目标靶点,模型一致性高,数据可重复性强。
- 高适用性
无论是构建BBB共培养模型、验证靶向递送系统,还是研究神经元特异性摄取机制,均可提供稳定可靠的细胞基础。
- 高灵敏度
靶点高表达意味着对药物/纳米载体的响应更灵敏,更易捕捉到差异信号,降低假阴性风险。
- 稳定性高
赛业生物的皮质神经元为批次生产的细胞现货,细胞一致性高,特异性marker表达高且均一,批次间数据重复性强,可信度高。
成熟的皮质神经元明场图片:

明场显微镜下,iPSC皮质神经元呈现典型的神经元形态:胞体呈圆形或椭圆形,折光性良好,边界清晰;从胞体发出细长、光滑的轴突和多个分支的树突,轴突延伸较长且末端可见生长锥,树突呈逐渐变细的锥形结构。随着培养时间延长,神经元之间形成密集的神经纤维网络,细胞间通过突触样结构相互连接,整体呈现均一、立体感强的生长状态,无明显细胞碎片或空泡化。
免疫荧光验证皮质神经元特异性标志物:
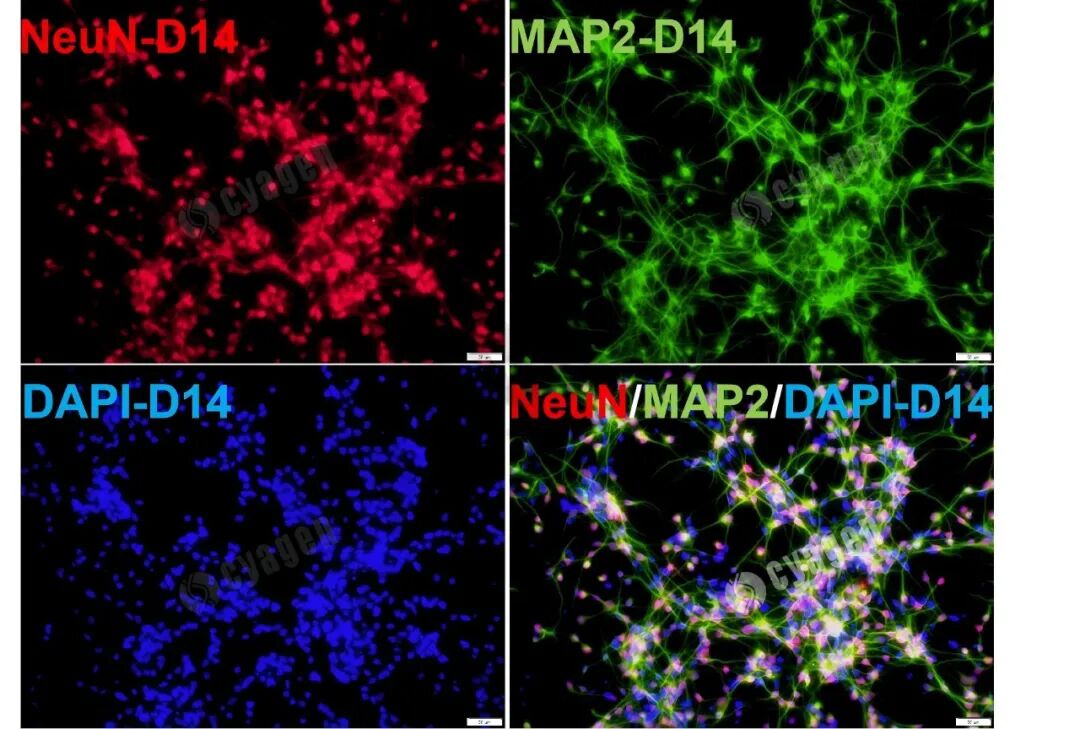
免疫荧光染色显示iPSC分化的皮质神经元(第14天)表达神经元特异性标志物NeuN(红色)和MAP2(绿色),细胞核由DAPI复染(蓝色)。合并图显示NeuN与MAP2共定位,确认神经元身份及成熟状态。
电生理数据:

1)iPSC来源皮质神经元的电压门控钠/钾电流记录全细胞膜片钳记录显示,在去极化步阶刺激下,神经元产生典型的快速内向钠电流(向下deflection)和缓慢外向钾电流(向上deflection),表明功能性电压门控离子通道的表达。
2)iPSC来源皮质神经元诱发的动作电位在电流钳模式下,向神经元注入去极化电流脉冲可诱发单次或多次动作电位,显示神经元具备兴奋性和动作电位发放能力。
3)iPSC来源皮质神经元自发的动作电位在无外加刺激条件下,记录到神经元自发性动作电位发放,提示神经元具备自主电活动能力,进一步证实其功能成熟度。
赛业生物的皮质神经元能做什么?
BBB模型构建作为共培养体系的“神经元端”,诱导内皮细胞形成紧密连接,重现功能性屏障受体介导转胞吞研究TFR1高表达,适合验证转铁蛋白/抗体修饰的纳米粒跨BBB递送效率靶向肽/载体筛选CD98+TFR1双靶点,可用于双配体载体的结合效率评估、神经疾病机制研究、高质量皮质神经元,适用于AD、PD、脑卒中等疾病模型的体外药效验证。
填写需求描述给我们
工具快速咨询
400-680-8038
info@oricellbio.cn



