JEV丨南京大学团队开发靶向致病性囊泡的骨关节炎新疗法
骨关节炎(Osteoarthritis, OA)是一种以关节软骨进行性退化、滑膜炎症及骨赘形成为特征的退行性关节疾病,常导致慢性疼痛与运动障碍,发病率高,构成了沉重的医疗与社会经济负担。目前临床干预手段主要集中在症状缓解及终末期关节置换,尚缺乏能够延缓或逆转疾病进程的治疗方法。近年来研究表明,关节内细胞间的异常通讯是驱动OA进展的核心环节。其中,细胞外囊泡作为携带蛋白质、核酸等生物活性分子的纳米级载体,在病理信号传递中发挥关键作用。滑膜成纤维样细胞作为滑膜组织的主要基质细胞,在OA病理状态下常表现为炎症激活与细胞衰老。然而,此类病变FLS所释放的囊泡在OA进展中的具体作用机制及其靶向干预潜力,仍有待系统阐明。
2025年9月,南京大学医学院附属鼓楼医院运动医学与成人重建外科蒋青、郭保生、陈响教授团队在细胞外囊泡领域权威期刊Journal of Extracellular Vesicles(IF 14.5)上发表了题为“Targeted Blockage of Pathological Extracellular Vesicles and Particles From Fibroblast-Like Synoviocytes for Osteoarthritis Relief: Proteomic Analysis and Cellular Effect”的研究成果。该研究通过整合临床样本分析、动物模型验证及多组学技术,系统揭示了OA状态下炎症性与衰老性FLS来源的致病性囊泡(EVP)在多细胞层面驱动关节退变的机制,并创新性地开发了一种基于滑膜靶向性腺相关病毒载体的基因治疗策略,为OA的疾病修饰治疗提供了新思路。

文献截图
研究材料和方法
本研究中体外实验主要采用了从小鼠分离的原代软骨细胞、滑膜成纤维细胞、骨髓间充质干细胞(BMSC)以及脂肪来源间充质干细胞(ADSC),并使用RAW264.7单核巨噬细胞系和ATDC5软骨细胞系进行辅助研究;培养过程中,在MSC成软骨分化实验中使用了赛业生物OriCell®专用的成软骨诱导分化试剂盒(货号分别为MUXMX-90041、MUXMD-90041)。体内实验采用C57BL/6J小鼠,通过内侧半月板失稳术(DMM)构建了小鼠OA模型,用于评估靶向治疗策略的疗效与安全性。
技术路线
1. 组学与生物信息学分析方面:对FLS来源的EVP进行了高通量蛋白质组学分析;整合挖掘了GEO数据库中的转录组学数据,并利用生物信息学工具进行通路富集和网络分析。
2. 分子与细胞生物学技术包括:qPCR、Western Blot、ELISA、成软骨分化及阿利新蓝染色、免疫荧光染色、免疫组织化学染色、SA-β-gal衰老染色、EdU/TUNEL检测等。
3. 外泌体研究技术主要为:差速超速离心分离纯化、纳米颗粒追踪分析与透射电镜表征、以及荧光标记示踪内化实验。
4. 基因操作与递送技术包括:慢病毒介导的基因敲低和AAV载体构建与关节腔内注射。
5. 组织病理学评估:H&E、番红O固绿、甲苯胺蓝等染色。

图1. 技术路线
-
OA滑膜组织中外泌体分泌通路显著激活
通过分析OA患者与正常滑膜的转录组数据,研究发现与“细胞外囊泡”相关的生物学通路在OA组织中显著富集。关键调控基因RAB27A的表达在OA滑膜中明显上调,且与炎症标志物(IL6、MMP13)和衰老标志物(CDKN1A)的表达呈显著正相关。组织免疫荧光进一步证实,在OA滑膜组织中,RAB27A蛋白主要高表达于呈现炎症或衰老表型的滑膜成纤维样细胞中。体外实验表明,经炎症诱导或衰老诱导的FLS所分泌的EVP,在颗粒数量与蛋白总量上均显著高于正常FLS,提示病理状态下的FLS具有EVP高分泌的特征。
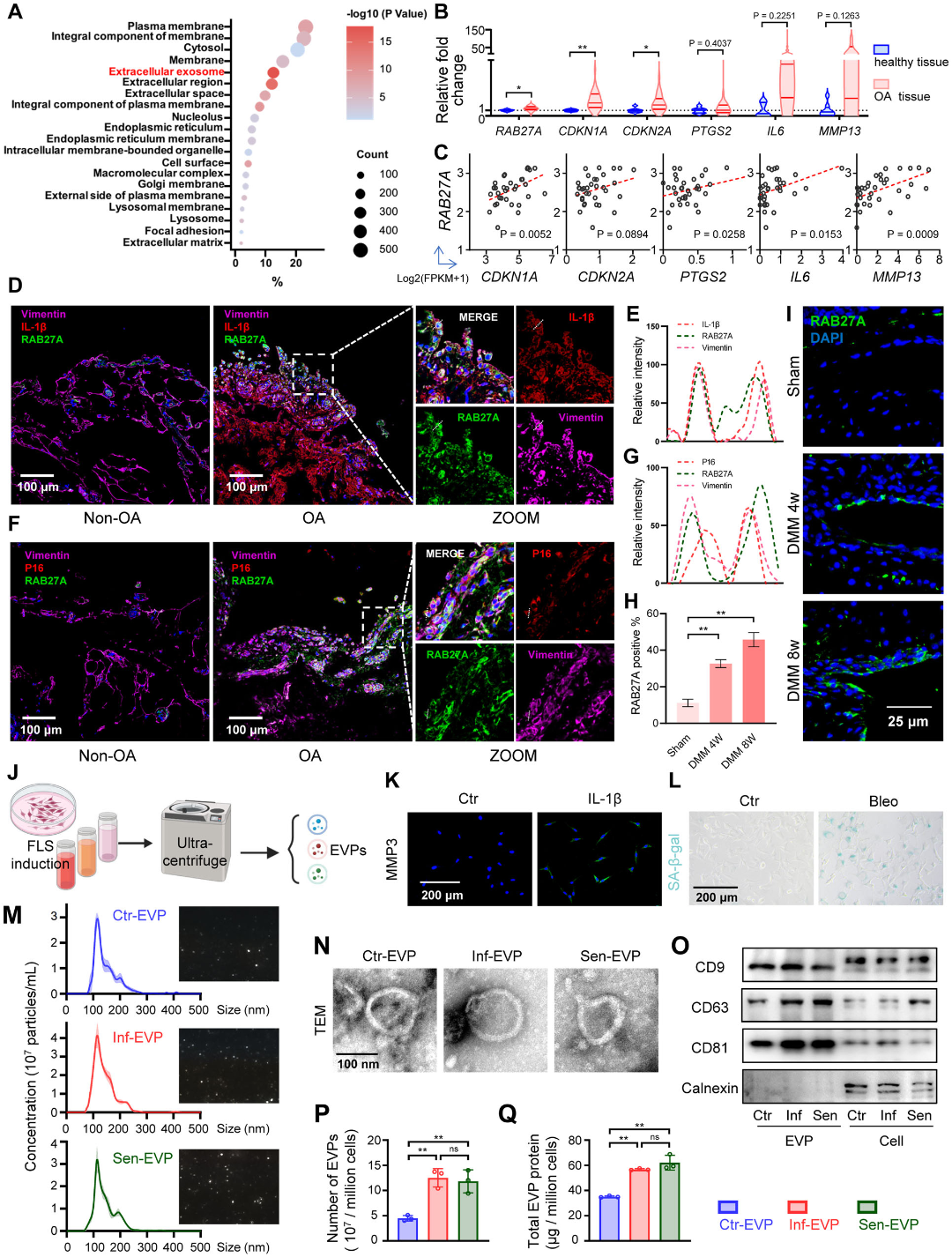
图2. OA滑膜与FLS中囊泡分泌显著增强
-
不同病理来源EVP具有特征性蛋白质组学图谱
研究对正常、炎症及衰老FLS来源的EVP进行了深度蛋白质组学分析。结果显示,三种EVP的蛋白组成存在显著差异,其中炎症性EVP富集了与炎症信号传导相关的蛋白,而衰老性EVP则主要富集了参与细胞周期调控和DNA修复过程的蛋白。这一发现表明,EVP的分子载荷能够精确反映其亲本细胞的病理状态,提示其可能作为疾病状态的信号载体参与细胞间通讯。通过对差异表达蛋白进行功能富集分析,研究发现致病性EVP中显著变化的蛋白主要参与软骨发育、胶原代谢以及炎症反应等生物学过程。进一步的整合分析表明,这些差异蛋白与公共数据库中OA软骨退变、间充质干细胞成软骨分化抑制以及巨噬细胞M1极化相关的基因集存在高度重叠,从生物信息学角度支持了致病性EVP可能通过多途径协同驱动OA进展的假说。
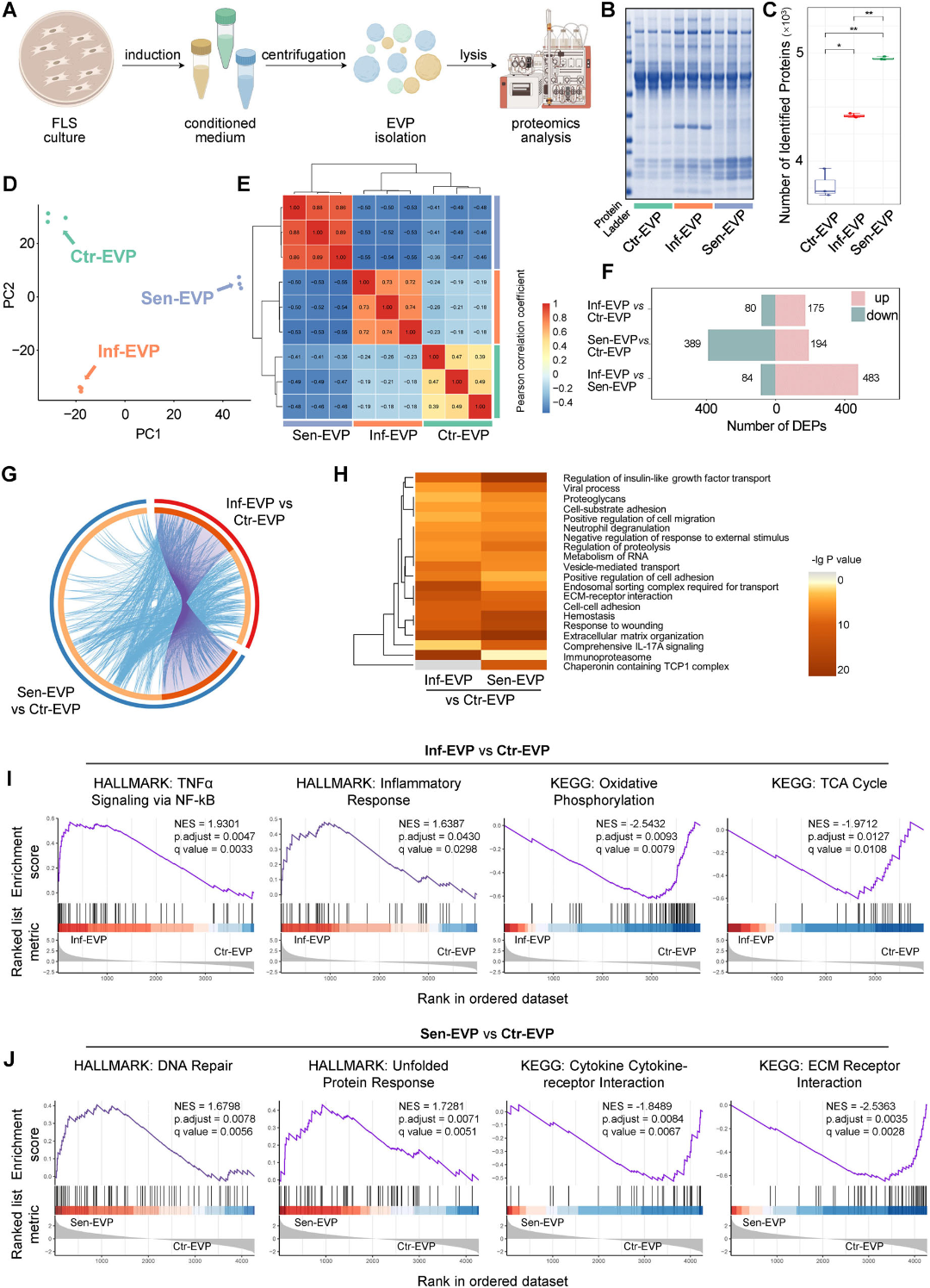
图3. 致病性EVP蛋白组成与OA病理进程密切相关
-
致病性EVP破坏软骨细胞稳态并驱动巨噬细胞向促炎表型极化
在细胞功能层面,研究发现炎症性与衰老性EVP可被软骨细胞有效内化,并诱导软骨细胞发生衰老、合成代谢抑制和分解代谢增强,同时伴随增殖能力下降和凋亡增加。在巨噬细胞中,致病性EVP同样被有效摄取,并诱导其向M1型促炎巨噬细胞极化,表现为M1标志物表达上调和促炎因子分泌增加。这些结果表明,致病性EVP能够直接破坏关节内两种关键细胞的正常功能,加剧局部炎症与组织破坏。
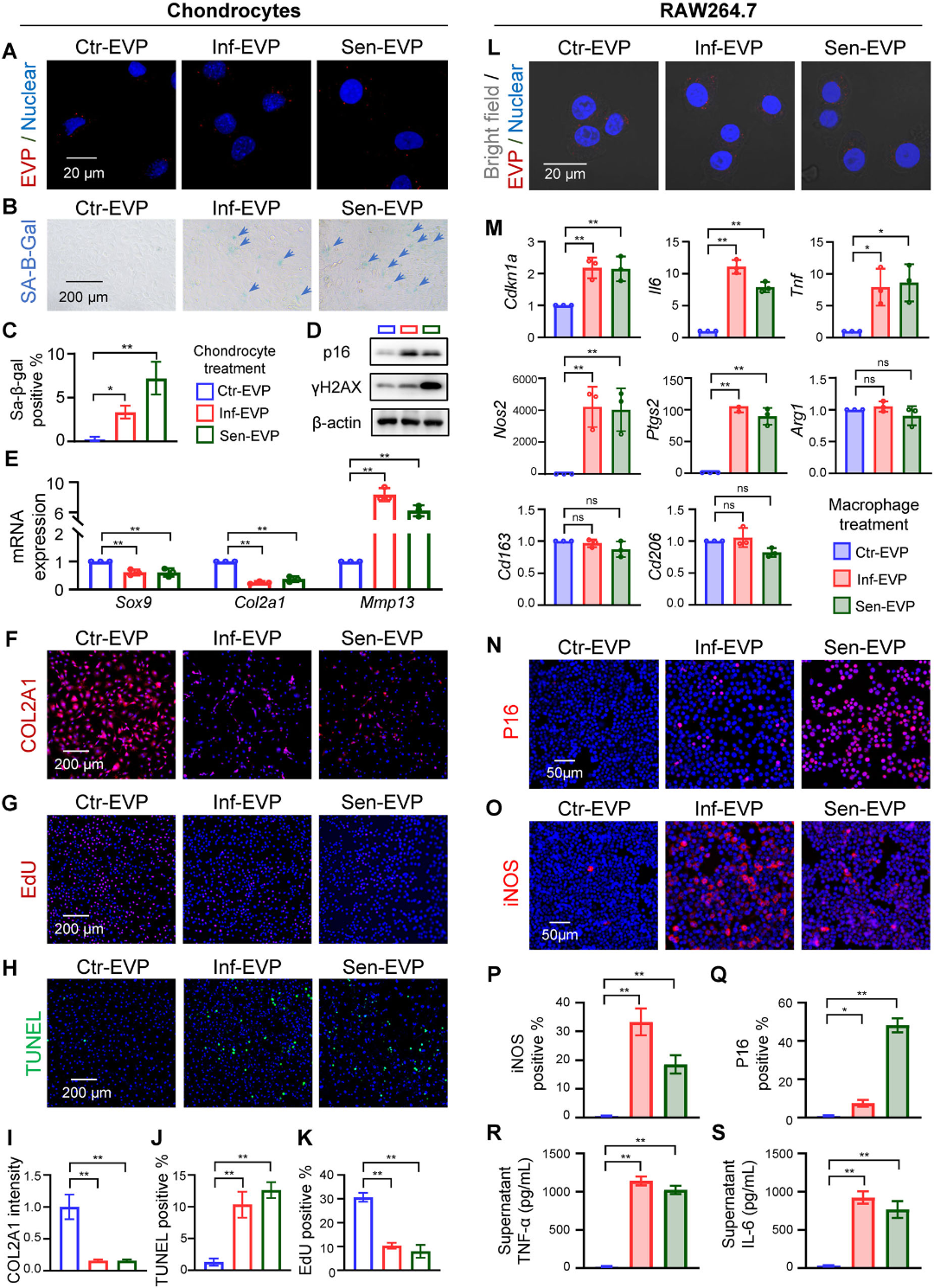
图4. 致病性EVP破坏软骨细胞稳态并诱导巨噬细胞M1极化
-
致病性EVP损害间充质干细胞的软骨向分化能力
研究进一步探讨了致病性EVP对关节内修复潜能的影响。实验发现,在炎症性或衰老性EVP存在的条件下,骨髓来源和脂肪来源的间充质干细胞其成软骨分化能力均受到显著抑制,表现为软骨球形成不良、软骨特异性基质合成减少以及成软骨关键转录因子SOX9表达下调,同时伴随肥大软骨细胞标志物COL10A1的表达升高。这一结果提示,OA关节腔内病理微环境中的致病性EVP可能严重削弱干细胞介导的内源性修复。
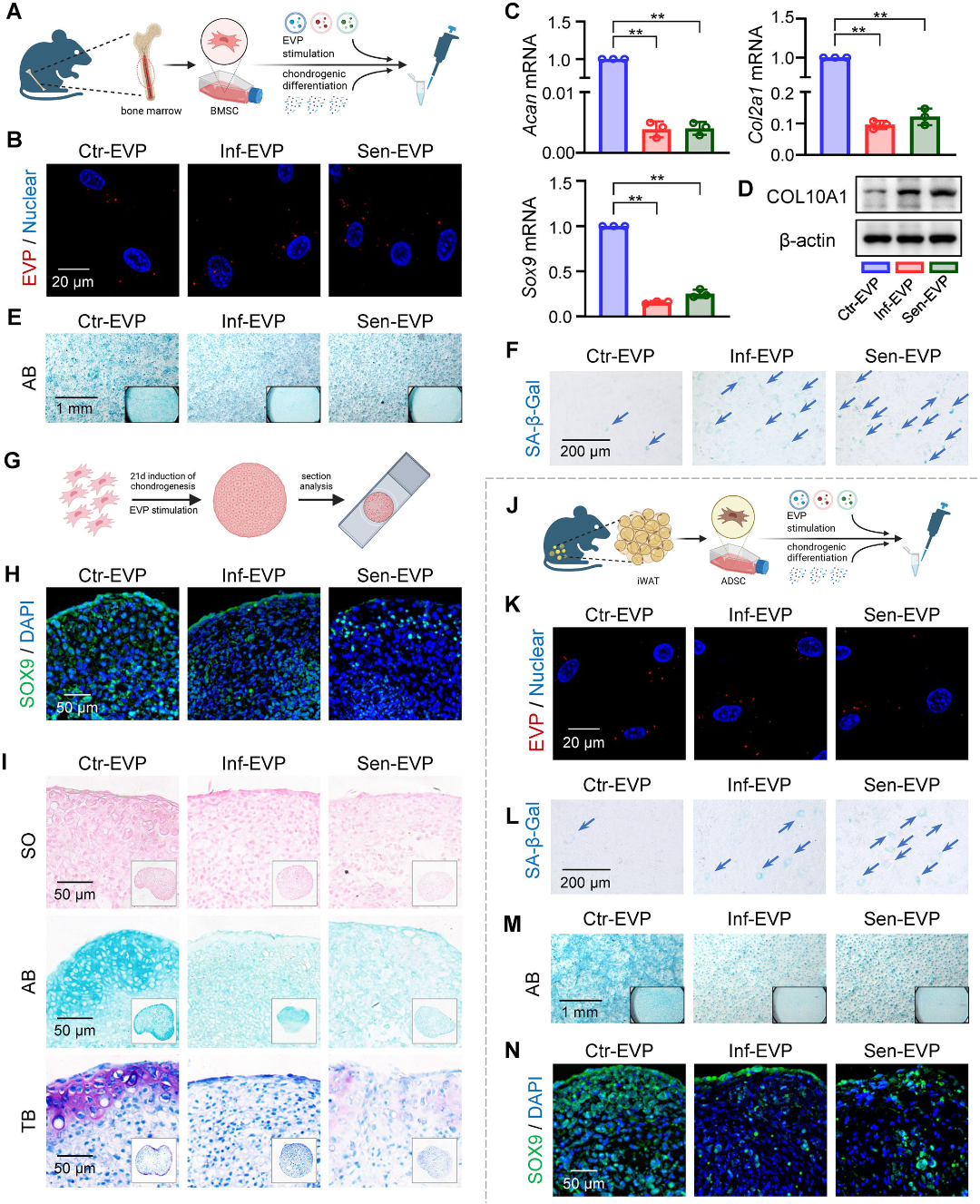
图5. 致病性EVP损害MSC的成软骨分化能力
-
靶向抑制RAB27A可有效阻断致病性EVP分泌并缓解OA病理进程
基于上述机制,研究开发了一种靶向治疗策略:通过构建携带滑膜靶向肽HAP-1的腺相关病毒载体,并在体内递送靶向Rab27a的shRNA,研究实现了对滑膜FLS中EVP分泌的特异性抑制。在OA小鼠模型中,该治疗能显著减轻软骨结构破坏、抑制滑膜增生并降低局部炎症水平。重要的是,该干预未引起明显的全身毒性,表明靶向抑制EVP分泌是一种兼具疗效与安全性的潜在OA治疗新策略。
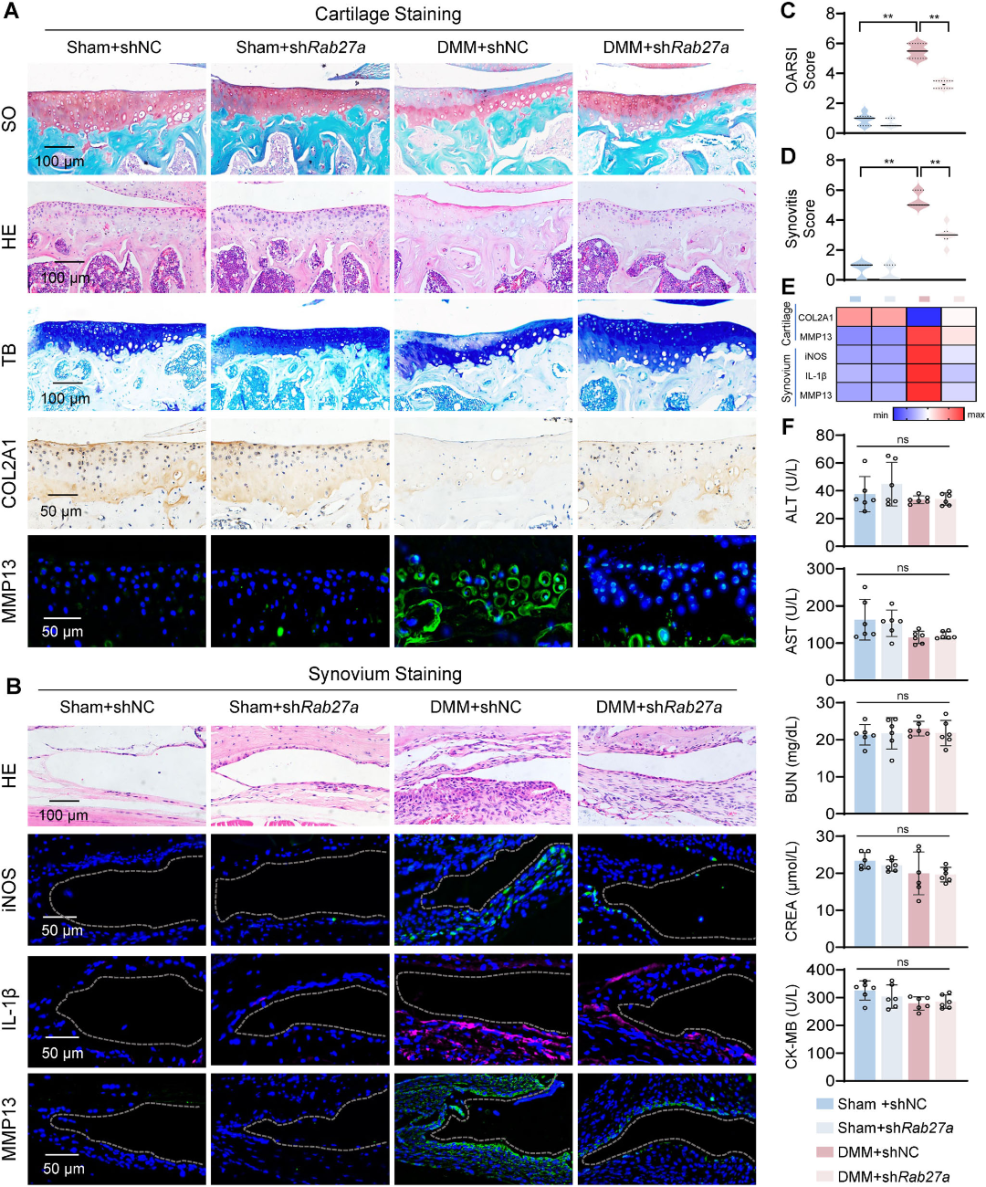
图6. 靶向抑制EVP分泌有效缓解OA且安全
研究总结
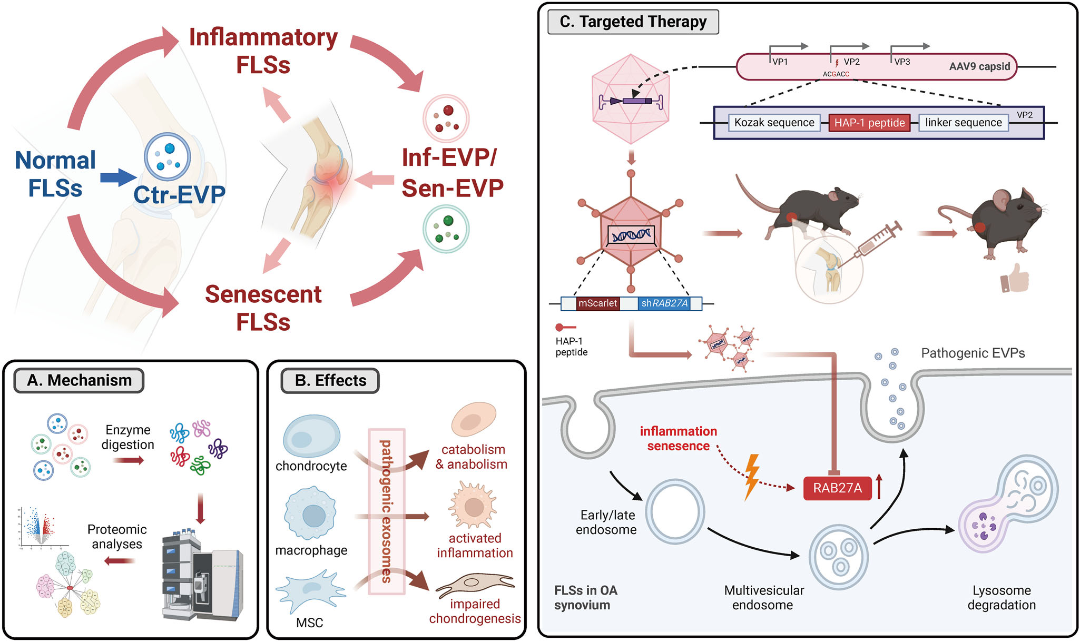
图7. 研究机制示意图
原文检索:
Liu, B., Xian, Y., Shen, T., Ben, Y., Wu, W., Shi, Y., An, X., Peng, R., Gao, W., Gong, W., Chen, X., Guo, B., & Jiang, Q. (2025). Targeted blockage of pathological extracellular vesicles and particles from fibroblast‐like synoviocytes for osteoarthritis relief: Proteomic analysis and cellular effect. Journal of Extracellular Vesicles, 14, e70162. https://doi.org/10.1002/jev2.70162
赛业生物OriCell干细胞诱导分化
赛业生物OriCell长期致力于干细胞领域的研究,在干细胞的诱导分化中有专业的技术及丰富经验,依赖于成熟的干细胞技术平台,我们可以提供多种干细胞向成骨诱导分化、成脂诱导分化、成软骨诱导分化的专用试剂,组分齐全、促高效分化;还可提供开展多种干细胞分化潜能研究的实验服务。
OriCell助力产品
|
引用产品 |
货号 |
|
MUXMX-90041 |
|
|
小鼠脂肪间充质干细胞成软骨诱导分化试剂盒 |
MUXMD-90041 |
成软骨诱导分化试剂盒含【细胞基础培养基+诱导添加物+阿利辛蓝染色液】,一套即可完成细胞诱导及染色鉴定。
填写需求描述给我们
工具快速咨询
400-680-8038
info@oricellbio.cn



