Biomaterials丨浙大一院开发可注射微凝胶搭载BMSCs及二甲双胍通过协同抗炎、抗氧化与再生作用促进软骨修复
关节软骨是一种无血管、无神经的结缔组织,再生能力有限,其损伤后的临床治疗面临挑战。传统微骨折手术无法提供足够的微环境来支持骨髓间充质干细胞定向分化为透明软骨。软骨损伤会引发急性炎症和活性氧增多,形成氧化应激恶性循环,严重阻碍愈合。二甲双胍作为常用降糖药,被发现能调节炎症和氧化损伤,但其在急性软骨缺损中的抗炎和再生作用尚不明确。
近日,来自浙江大学医学院附属第一医院许鉴研究团队在期刊Biomaterials(IF:12.9)上发表“Dual-loaded BMSCs-Metformin microgels promote cartilage repair through combined anti-inflammatory, antioxidant, and regenerative effects”相关研究文章,提出了一种创新的软骨修复策略。

本研究采用微流控技术制备了负载BMSCs和二甲双胍的微凝胶(BMSC-Met@MGs),该系统由三种材料组成,各发挥关键作用:
-
甲基丙烯酰化明胶(GelMA):促进细胞附着与增殖。
-
甲基丙烯酰化壳聚糖(CSMA):发挥抗菌抗炎作用并招募内源性细胞。
-
聚乙烯醇(PVA):增强力学性能并控制药物释放。
该体系通过持续释放二甲双胍及协同调控内外源BMSCs,展现出抗炎、抗氧化和促进软骨再生的综合功效。
研究材料和方法
技术路线
-
微凝胶的制备与表征
-
体外验证Met@MGs的促增殖与迁移能力
-
体外验证Met@MGs的促软骨分化能力
-
体外验证BMSC-Met@MGs的免疫调节作用及其机制
-
体外验证BMSC-Met@MGs的抗氧化活性
-
体内验证BMSC-Met@MGs的软骨缺损修复效果
关键研究结果
-
微凝胶的制备与表征
为了构建一种可注射的递送系统,研究团队采用微流控技术成功制备了由明胶甲基丙烯酰胺(GelMA)、壳聚糖甲基丙烯酰胺(CSMA)和聚乙烯醇(PVA)组成的多孔微凝胶(MGs)。傅里叶变换红外光谱(FTIR)分析证实了PVA和二甲双胍(Met)通过氢键成功引入到凝胶网络中。流变学分析表明,前体溶液在紫外光照射下可在3秒内迅速发生凝胶化。扫描电子显微镜(SEM)显示微凝胶具有高度多孔的内部结构。体外降解实验表明,微凝胶在胶原酶II溶液中可持续降解超过6周。药物释放曲线显示,Met在初始3天快速释放后,能在28天内实现持续释放(累计释放率78.63%)。此外,活/死细胞染色和细胞骨架染色证实,封装在微凝胶中的BMSCs存活率高、形态舒展,表明该微凝胶具有良好的生物相容性,能为细胞提供适宜的微环境。
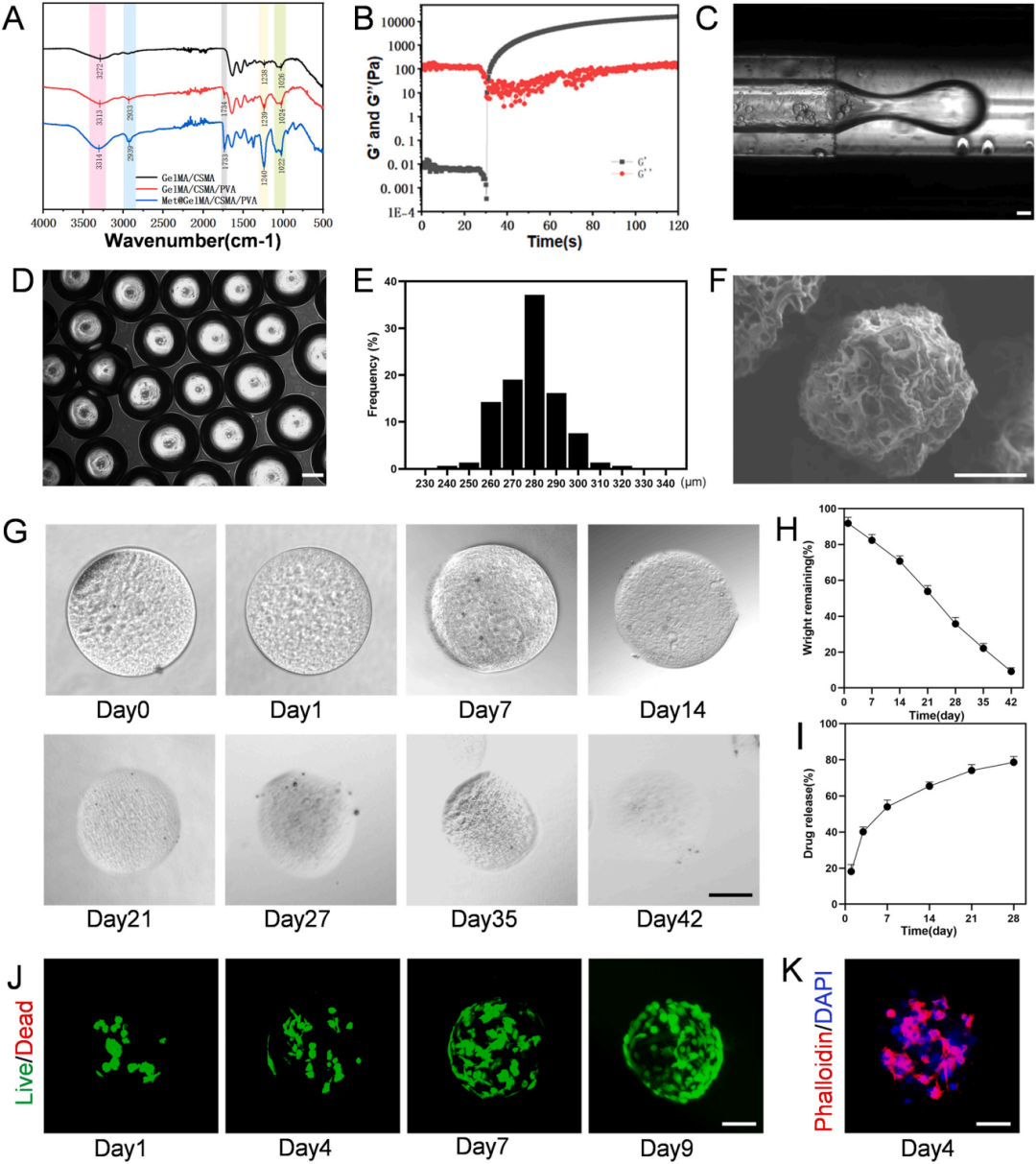
图1. 复合材料和微凝胶(MGs)的制备及表征
-
Met@MGs增强细胞增殖与迁移能力
研究团队通过CCK-8实验、Transwell实验和细胞划痕实验,系统评估了Met、MGs及其复合物(Met@MGs)对BMSCs和软骨细胞行为的影响。CCK-8结果表明,在与微凝胶共培养7天后,Met和Met@MGs能显著促进BMSCs和软骨细胞的增殖。Transwell和划痕实验结果显示,与对照组、单独MGs或Met组相比,Met@MGs处理组能最有效地诱导BMSCs和软骨细胞的定向迁移,并加速划痕区域的闭合。这些结果表明,Met@MGs不仅能促进关键修复细胞的增殖,还能有效招募它们向损伤区域迁移。
图2. Met@MGs可有效促进体外BMSCs及软骨细胞的增殖与迁移
-
Met@MGs促进BMSCs的软骨向分化
为了评估微凝胶环境对干细胞分化的影响,研究团队将封装有BMSCs的MGs和Met@MGs在软骨诱导培养基(大鼠骨髓间充质干细胞成软骨诱导分化试剂盒,赛业生物OriCell®,货号RAXMX-90041)中培养14天。通过免疫荧光染色和RT-qPCR对软骨形成相关标志物进行检测。结果显示,与未加载Met的MGs组相比,Met@MGs组中软骨特异性细胞外基质成分II型胶原(COL2A1)的蛋白和基因表达水平显著上调,而I型胶原(COL1A1)和X型胶原(COL10A1)的表达则被显著抑制。同时,成熟软骨细胞标志物聚集蛋白聚糖(ACAN)和转录因子SOX9的mRNA表达也显著升高。这表明Met与微凝胶协同作用,能有效引导BMSCs向透明软骨分化,并抑制纤维化及肥大化等不良分化路径。
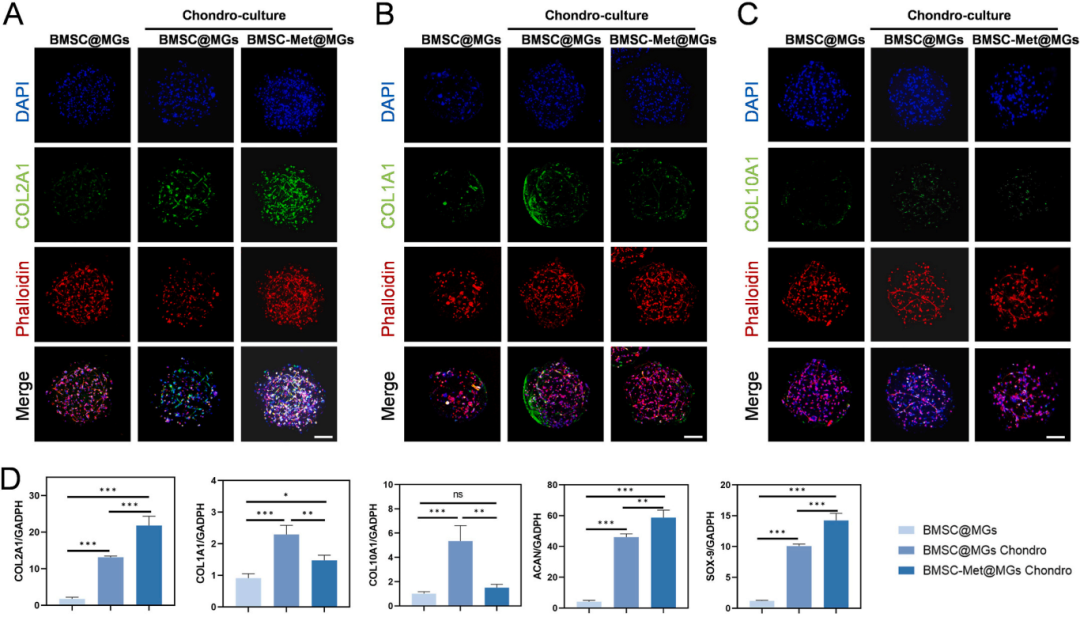
图3. MGs和Met@MGs负载BMSCs的体外促成软骨分化作用
-
BMSC-Met@MGs的免疫调节作用
研究团队在体外使用白细胞介素-1β(IL-1β)刺激软骨细胞以模拟损伤后的炎症微环境,并探究BMSC-Met@MGs的免疫调节功能。阿尔新蓝染色和糖胺聚糖(GAG)含量测定表明,BMSC-Met@MGs能有效逆转IL-1β引起的细胞外基质流失。免疫荧光和RT-qPCR分析显示,该治疗组能显著降低炎症因子IL-1β诱导的基质金属蛋白酶(MMP3和MMP13)的表达,同时维持较高的COL2A1水平。进一步的RNA测序(mRNA-seq)和通路富集分析发现,BMSC-Met@MGs处理后,与炎症相关的NF-κB、TNF和IL-17等信号通路被显著抑制。Western Blot和免疫荧光实验证实,BMSC-Met@MGs能抑制IL-1β诱导的NF-κB p65亚基的磷酸化及核转位。这些结果从分子层面揭示了其通过抑制NF-κB通路发挥抗炎和保护软骨作用的机制。
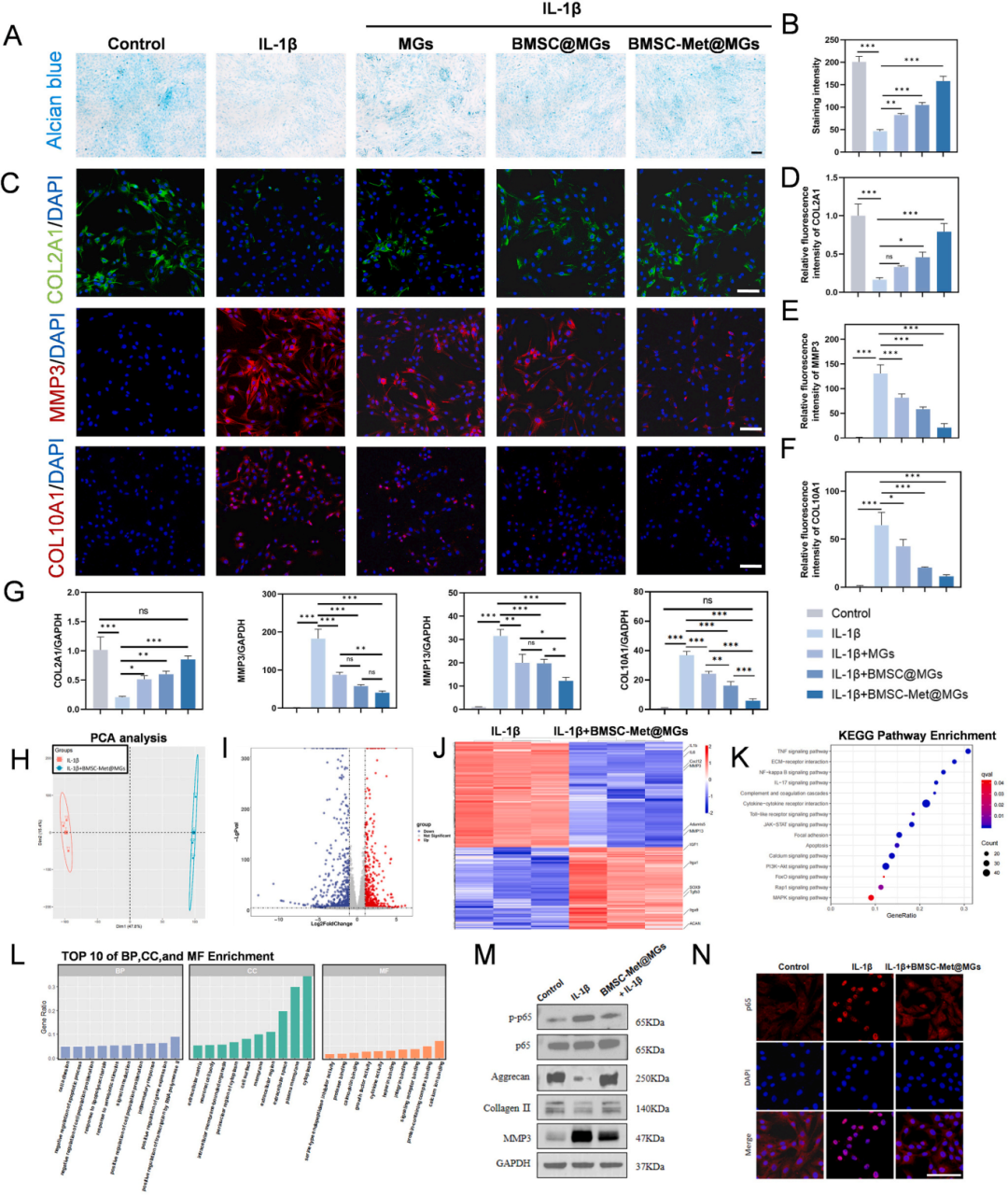
图4. BMSC-Met@MGs对软骨细胞的体外免疫调节作用及mRNA测序机制研究
-
BMSC-Met@MGs的抗氧化活性
研究团队利用过氧化氢(H₂O₂)处理软骨细胞构建氧化应激模型,以评估BMSC-Met@MGs的抗氧化能力。通过DCFH-DA荧光探针检测细胞内活性氧(ROS)水平,发现BMSC-Met@MGs能最有效地清除H₂O₂诱导产生的过量ROS。使用JC-1染料评估线粒体膜电位的结果表明,BMSC-Met@MGs处理能显著恢复因氧化应激而降低的线粒体膜电位,减少线粒体功能受损的细胞比例。流式细胞术分析进一步定量验证了其在降低ROS水平和减少早期凋亡细胞方面的卓越效果。这表明BMSC-Met@MGs能有效缓解氧化应激,保护软骨细胞免受氧化损伤。
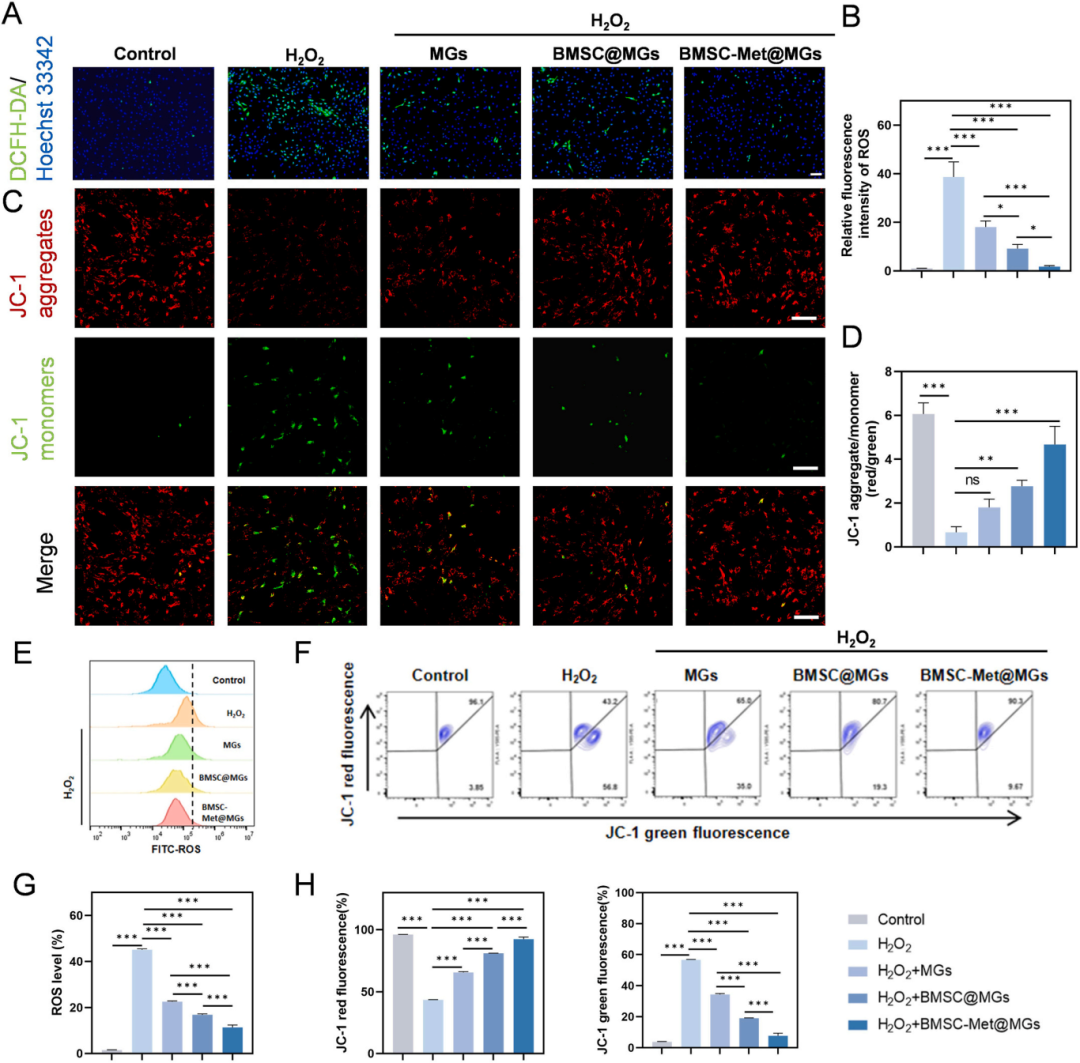
图5. BMSC-Met@MGs在软骨细胞中表现出抗氧化作用,并调节线粒体功能
-
BMSC-Met@MGs在大鼠软骨缺损模型中的修复效果
最后,研究团队在大鼠股骨滑车沟全层软骨缺损模型中评估了BMSC-Met@MGs的体内修复效能。活体成像显示,载有荧光标记的微凝胶和药物能在关节缺损部位滞留超过4周,实现了长效作用。术后8周的宏观观察和国际软骨修复协会(ICRS)评分显示,BMSC-Met@MGs组缺损修复效果最佳,表面光滑且与周围组织整合良好。组织学染色(H&E、番红O固绿、阿尔新蓝)表明,该组再生组织为典型的透明样软骨,具有丰富的GAG和COL2A1,且肥大软骨标志物COL10A1表达极低。显微CT(Micro-CT)分析显示其能促进软骨下骨的良好重建。步态分析和生物力学测试进一步证实,BMSC-Met@MGs治疗能显著改善关节功能,并使再生软骨的力学性能接近正常软骨。
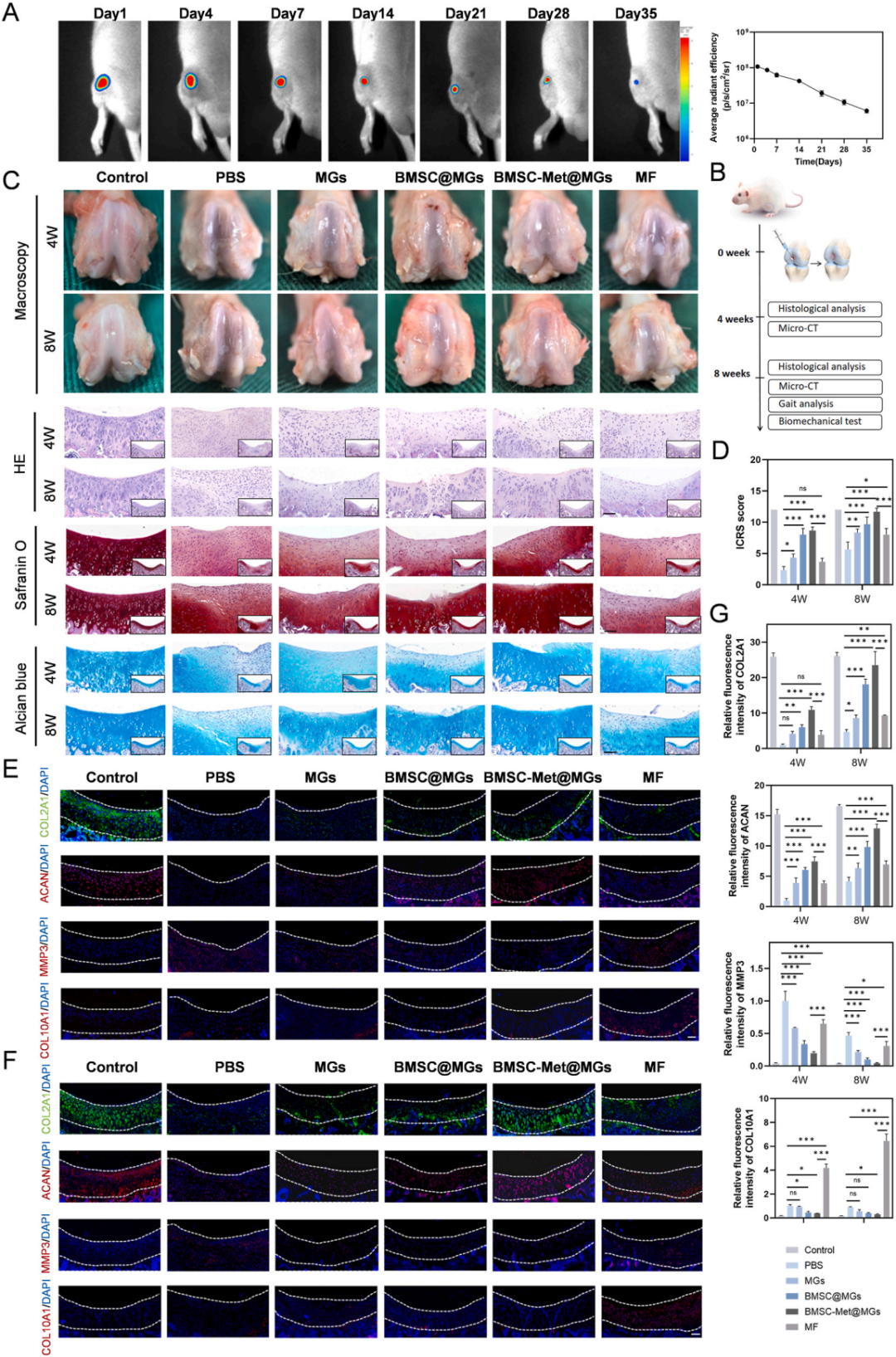
图6. BMSC-Met@MGs在大鼠软骨缺损模型中促进软骨修复(宏观和组织学水平)
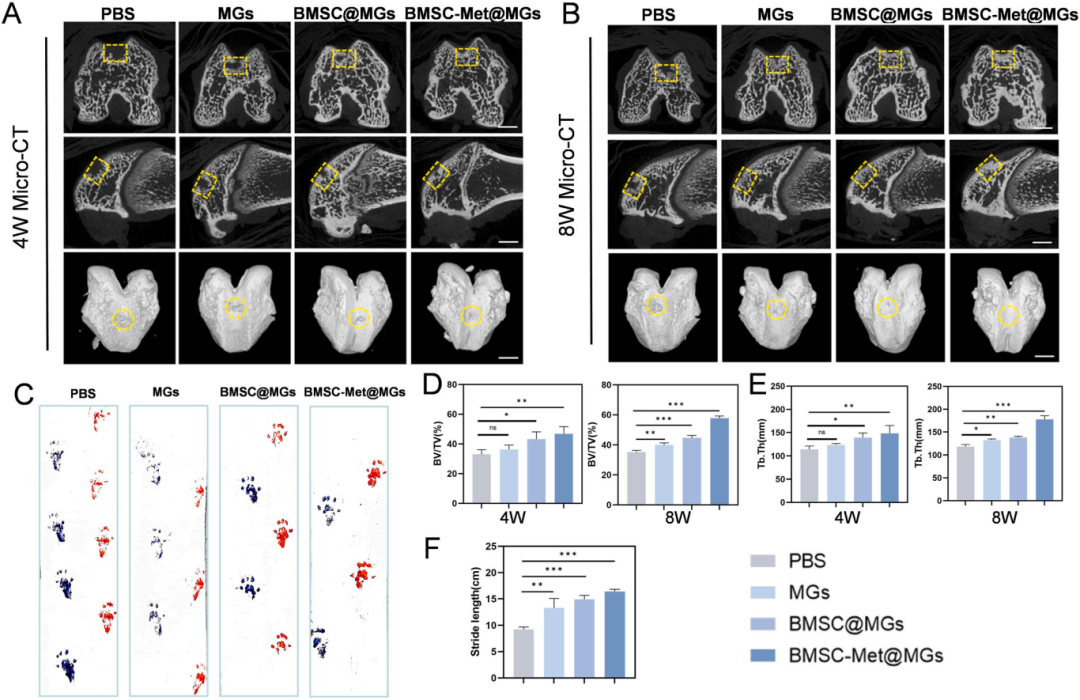
图7. 通过Micro-CT和步态分析对大鼠软骨缺损模型软骨再生和功能恢复进行综合评价
研究总结
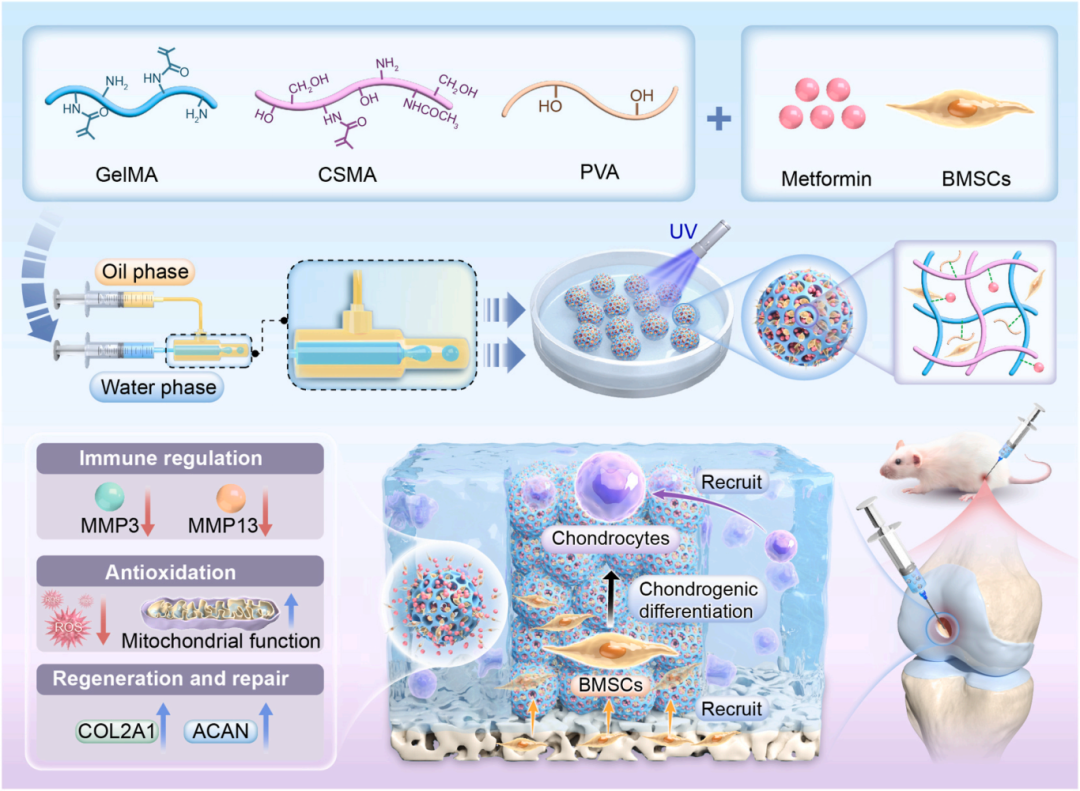
本研究成功开发了一种可注射的BMSC-Met@MGs微凝胶系统,通过协同材料、药物与细胞三方作用,首次实现了对软骨缺损的综合性治疗。
该体系在体内外均证实具有三重功效,为临床软骨再生提供了一种创新的治疗策略:
1. 有效抑制炎症反应并清除活性氧,改善损伤微环境。
2. 显著促进软骨基质合成与干细胞成软骨分化。
3. 成功修复软骨缺损,恢复关节功能。
原文检索:Li, D, Wang, Y, Yuan, G, et al. Dual-loaded BMSCs-Metformin microgels promote cartilage repair through combined anti-inflammatory, antioxidant, and regenerative effects. BIOMATERIALS. 2025; 328. doi:10.1016/j.biomaterials.2025.123805
赛业生物OriCell®干细胞诱导分化
赛业生物OriCell®长期致力于干细胞领域的研究,在干细胞的诱导分化中有专业的技术及丰富经验,依赖于成熟的干细胞技术平台,我们可以提供多种干细胞向成骨、成脂、成软骨分化的专用试剂,组分齐全、促高效分化;还可提供开展多种干细胞分化潜能研究的实验服务。
OriCell®助力产品
|
引用产品 |
货号 |
|
RAXMX-90041 |
填写需求描述给我们
工具快速咨询
400-680-8038
info@oricellbio.cn