IF 20.3!浙江大学医学院附属第一医院胡懿郃、谢杰团队:尿液干细胞外泌体逆转骨溶解
人工关节置换术是人工关节替代病变关节的过程,临床上主要应用于因关节退变、炎性关节病或创伤等导致正常关节结构功能丧失的患者。人工关节置换手术致力于治疗关节疾患、解除关节疼痛并重建关节功能,关节置换是终末期关节疾病的首选方法与最终手段。据统计,数百万例初次关节置换手术发现10年后的关节翻修率约为4-6%,每百万例全髋关节置换术中15年内的关节翻修率约为10%。全关节置换术后翻修手术最常见原因是关节假体与骨骼交界面发生的非感染性松动,即假体无菌性松动,术后10年的发生率约为10%,占所有翻修手术的30%以上。假体无菌性松动的非手术治疗效果不佳且再次翻修手术费用高,因此迫切需要进一步明确假体无菌性松动的发病机制并探讨临床防治策略。
近日,浙江大学医学院附属第一医院胡懿郃、谢杰团队,成功开发了一种融合外泌体(f-exo)系统,通过融合M2巨噬细胞来源外泌体(M2-exo)与尿液干细胞外泌体(USC-exo),实现假体周围骨溶解区域的靶向治疗及骨代谢稳态调控。文章发表于《Bioactive Materials》(IF 20.3),其介绍了一种超声联合脂质体挤压法制备融合外泌体的技术,将M2巨噬细胞来源外泌体(M2-exo)与尿液干细胞外泌体(USC-exo)融合为均一稳定的纳米颗粒(f-exo)。蛋白质组学研究表明,f-exo保留了M2-exo与USC-exo两种囊泡的蛋白组分,实现了对骨溶解病灶的靶向递送,精准调控了骨溶解区域的骨稳态微环境。

图1. 文献封面截图
研究材料:赛业OriCell®大鼠骨髓间充质干细胞成骨诱导分化试剂盒(货号RAXMX-90021),trap染色试剂盒,transwell系统等。
技术方法:
-
提取M2巨噬细胞来源外泌体(M2-exo)与尿液干细胞外泌体(USC-exo)制备并表征纳米颗粒(f-exo)。
-
通过体外实验验证了f-exo具有强大的促进成骨分化、血管生成,抑制破骨分化的能力。
-
体内实验表明f-exo具有靶向调节骨溶解病灶的骨稳态能力。
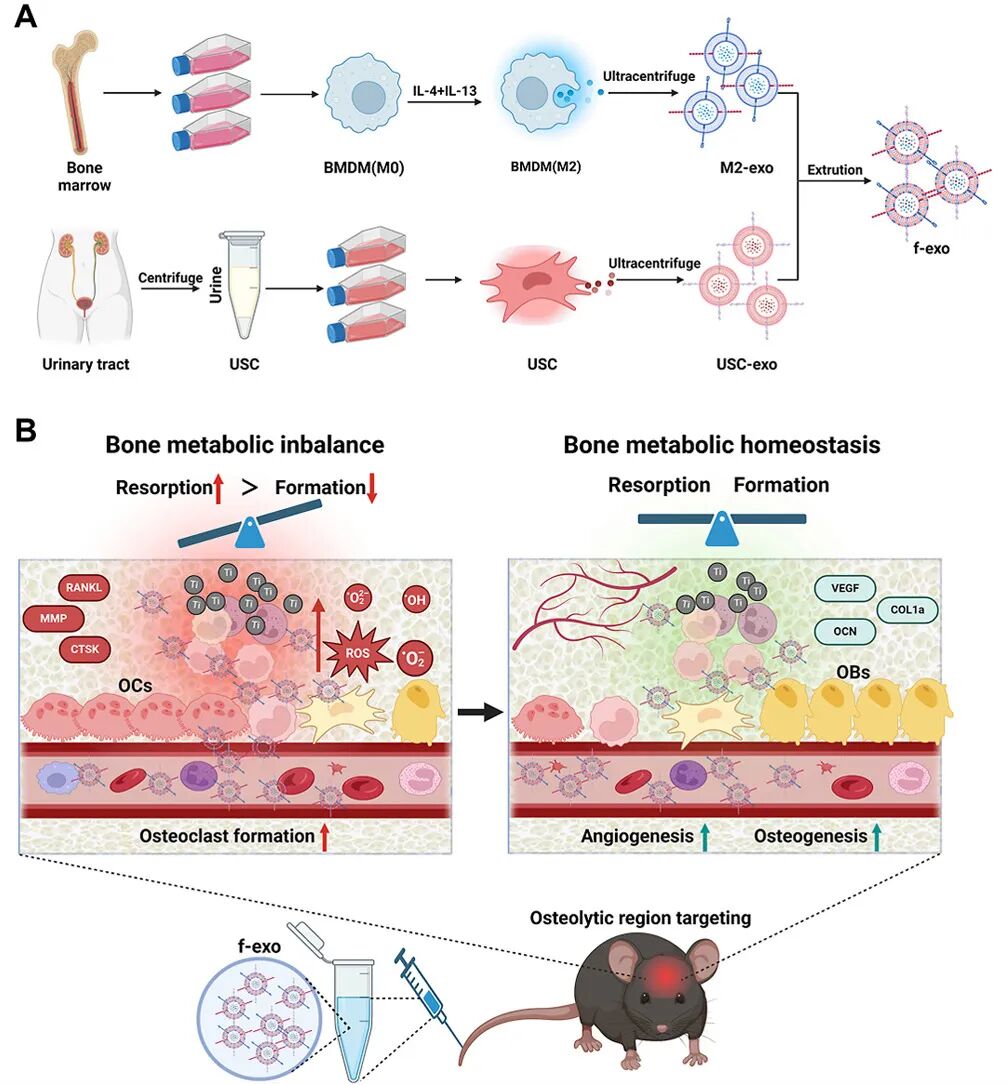
图2. (A) f-exo制备;(B) f-exo靶向调节骨溶解病灶的骨稳态机制。
本研究基于外泌体的磷脂双分子层结构,利用外泌体融合技术,原创性地提出并成功构建了M2-EXO递送USC-EXO的药物靶向递送系统,解决了USC-EXO在体内应用时面临的骨溶解部位靶向问题。同时构建的f-exo可以协同发挥两种外泌体的治疗效果调控骨代谢稳态,最终成功将f-exo应用于假体周围骨溶解稳态的靶向防治,取得了一系列原创性的结果。
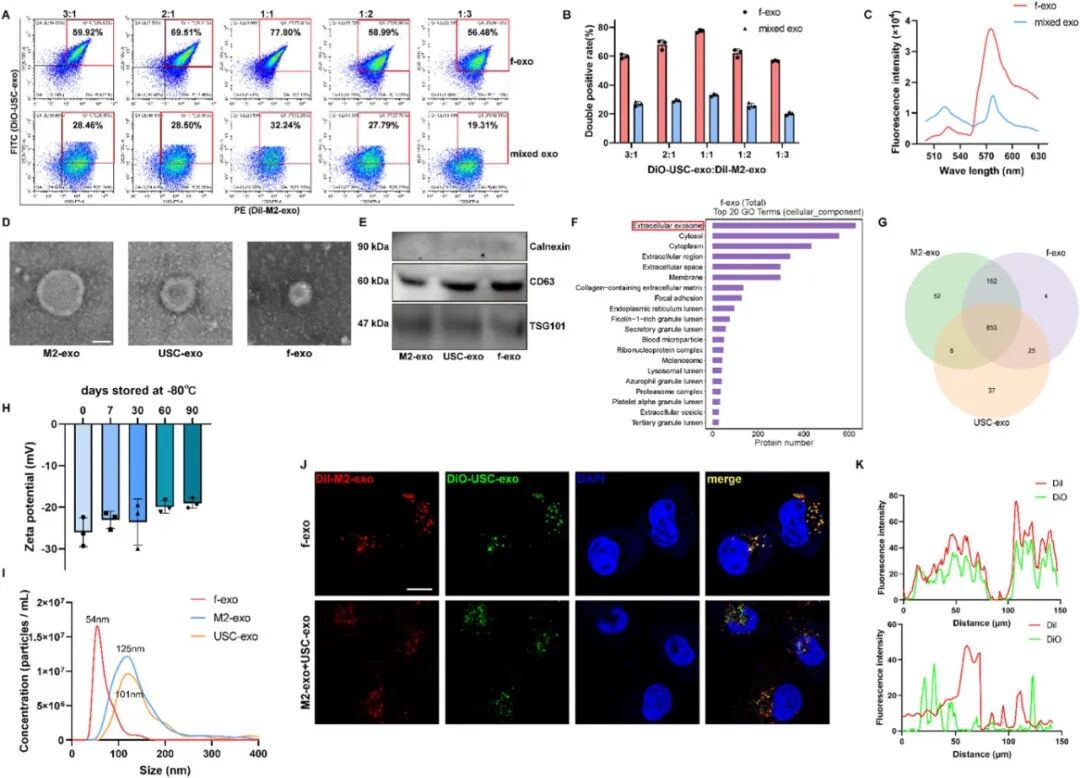
图3. f-exo的制备表征,通过WB、NTA、TEM等主要手段鉴定exo。
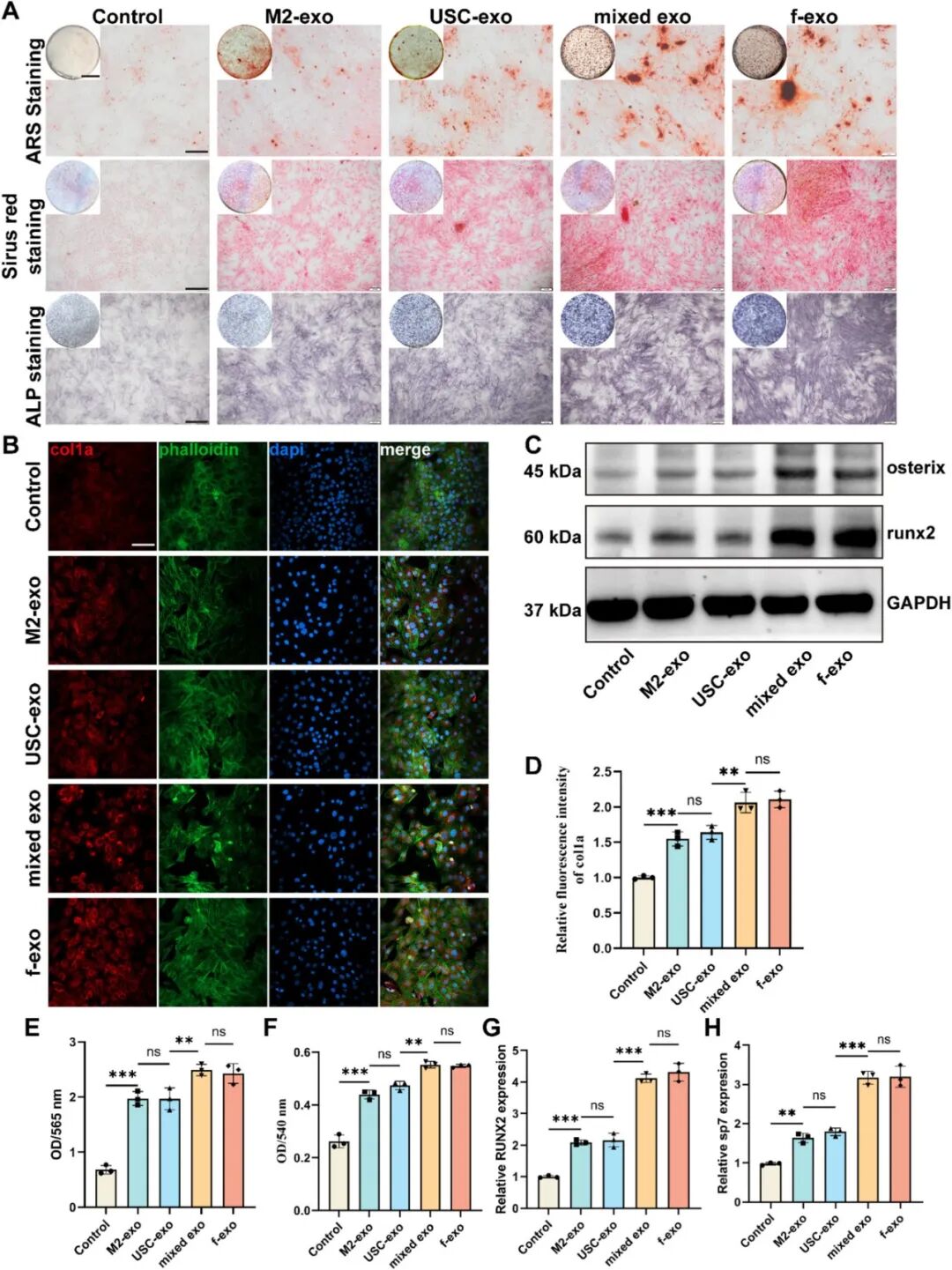
图4. f-exo体外成骨诱导实验,通过茜素红、天狼猩红、碱性磷酸酶染色验证f-exo对BMSC成骨分化的影响。其中使用了赛业OriCell®骨髓间充质干细胞成骨诱导分化试剂盒及其中配置的茜素红染色液,验证了f-exo在体外具有促进成骨能力。
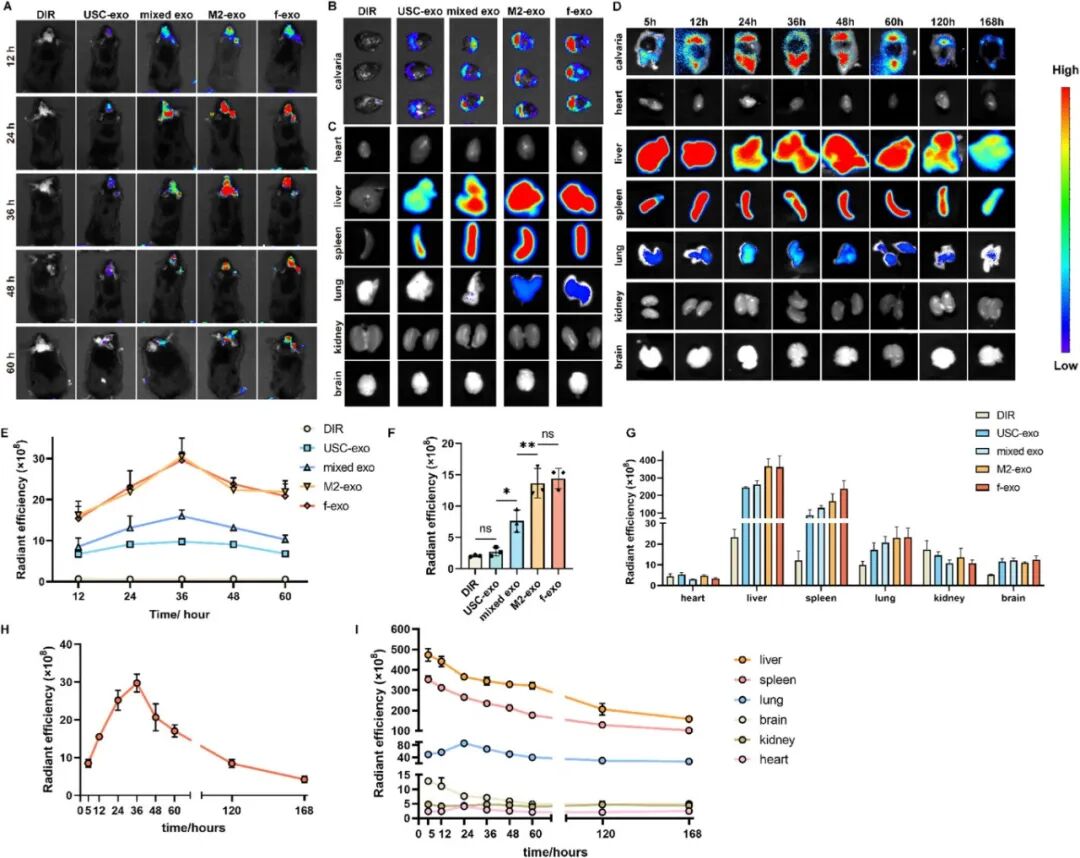
图5. f-exo具有更好的骨溶解区域靶向性,通过构建钛颗粒诱导的小鼠颅骨溶骨模型。通过尾静脉注射DiR标记的f-exo,并借助IVIS成像系统进行体内荧光成像,监测f-exo在体内的分布。
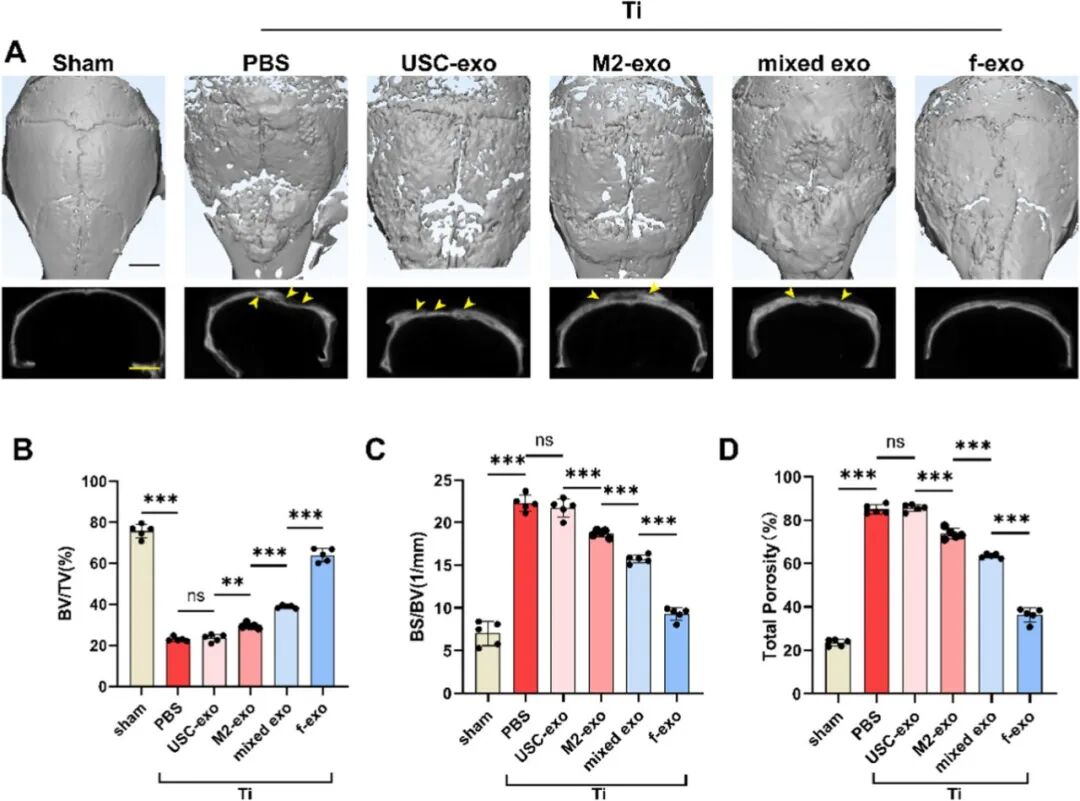
图6. 小鼠颅骨骨溶解模型Micro-CT图像。结果表明f-exo靶向调节了骨溶解区域的骨稳态代谢,抑制了钛磨损颗粒诱导的骨溶解。
原文检索:
[1] Ma T, Liu Q, Zhang Z, Nan J, Liu G, Yang Y, Hu Y, Xie J. Fused exosomal targeted therapy in periprosthetic osteolysis through regulation of bone metabolic homeostasis. Bioact Mater. 2025 Apr 8;50:171-188. doi: 10.1016/j.bioactmat.2025.04.006. PMID: 40248188; PMCID: PMC12005309.
填写需求描述给我们
工具快速咨询
400-680-8038
info@oricellbio.cn



