定制微凝胶开创新途径,助力骨软骨再生挑战
关节骨软骨单元由关节软骨、钙化软骨和软骨下骨三部分组成,具有复杂的软骨-骨界面,且不同组织层之间的特性不同。由于很难诱导间充质干细胞(MSC)向软骨和骨进行定向的可控分化,因此骨软骨单元的再生一直颇具挑战性。
近年来,类器官(organoids)技术迅速发展,为骨软骨再生提供了新的机会。然而,目前的主要局限是单一的支架和特定的培养基无法培养出具有异质性结构的类器官。采用其他方法尝试加入诱导生长因子,以诱导间充质干细胞定向分化,但也面临着实验成本高、细胞易失活等问题。
对此,北京大学人民医院和清华大学领导的研究团队利用定制的微凝胶开发出一种自组装的类器官,用于骨软骨再生。这种类器官呈现出分层组织结构,且无需使用大块支架或生长因子。这项成果已发表在《Bioactive Materials》杂志上,为推进组织工程领域的发展开辟了一条大有潜力的新途径。

01 研究材料和方法
研究人员设计并构建了透明质酸和羟基磷灰石修饰的明胶基微凝胶,之后将MSC(人脐带间充质干细胞)接种到这些定制的微凝胶中,诱导其分化为软骨细胞和骨细胞(成软骨诱导培养基和成骨诱导培养基由赛业OriCell®提供),之后通过自组装形成骨软骨类器官。然后通过扫描电镜、qRT-PCR、mRNA-seq等方法对骨软骨类器官进行了体外分析。最后将预分化的微凝胶注入比格犬的骨软骨缺损处,在术后3个月和6个月对所有膝关节进行采集分析。
制备CH-微凝胶和OS-微凝胶,将MSC接种到这些微凝胶中,诱导其分化为软骨细胞和骨细胞。
将预分化的成软骨和成骨微凝胶依次沉积为两层,通过自我组装形成骨软骨类器官。
通过mRNA-seq分析确定微凝胶中的MSC定向分化为软骨细胞和骨细胞的机制。
将预分化的微凝胶依次注射到比格犬的骨软骨缺损处,评估骨软骨类器官的体内修复能力。
02 研究结果
定制微凝胶的制备思路
前期研究发现,可注射的微凝胶(microcryogels)提供了一种3D微环境,可用来加载基质、细胞和生物活性因子,为各种实验模型的组织修复创造量身定制的细胞生态位。含有MSC的微凝胶可通过自我组装形成3D功能组织,提高MSC的干性和旁分泌活性。为了进一步改善MSC微凝胶中细胞的成软骨表型,研究人员故决定采用化学交联策略。
为了给MSC的成软骨分化和成骨分化提供合适的微环境,研究人员在基于明胶的前体溶液中分别加入透明质酸(HA)和羟基磷灰石(HYP),经过冷冻、铺板、洗涤和冻干后形成CH-微凝胶(用于成软骨分化)和OS-微凝胶(用于成骨分化)。之后将MSC接种到这些定制的CH-微凝胶和OS-微凝胶中,分别在成软骨诱导培养基和成骨诱导培养基中培养7天,再将预分化的成软骨和成骨微凝胶依次沉积为两层,通过自我组装形成骨软骨类器官(图1)。
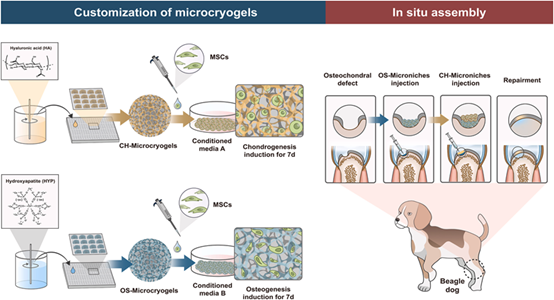
定制微凝胶的制备示意图[1]
将定制微凝胶自组装成骨软骨类器官
在自组装之前,研究人员首先评估了定制微凝胶中的成软骨和成骨分化。染色结果显示,与对照微凝胶相比,CH-微凝胶诱导成软骨分化的能力更强,而OS-微凝胶具有很强的促成骨分化的能力。CH-微凝胶中的成软骨标志物(COL2和SOX9)表达量较高,OS-微凝胶中的RUNX2基因表达量较高,但其他成骨分化基因(COL1、OCN和ALP)的表达量并无差异。
之后,研究人员将预分化的微凝胶移入边长4mm的网状框架内,并在骨软骨诱导混合培养基(成软骨分化:成骨分化=1:1)中培养7天。在预分化的微凝胶自组装成骨软骨类器官后,研究人员开展了体外分析(图2)。扫描电镜成像结果显示,整个类器官呈多孔结构,软骨成分和骨成分之间的界面整合良好。细胞追踪显示,自组装的类器官包含两层细胞,分别位于CH-微凝胶和OS-微凝胶中,这两层细胞很好地整合在一起,没有融合成一团细胞。有趣的是,两种定制微凝胶促进血管生成的能力不同。CH-微凝胶中没有新生血管,而OS-微凝胶中有许多血管生长,表明OS-微凝胶有更好的促进血管生成的潜力。
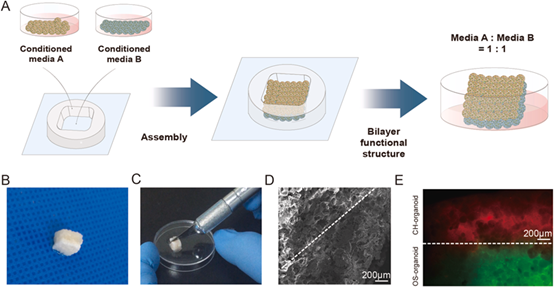
骨软骨类器官的体外自组装[1]
定制微凝胶指导MSC的命运
接下来,研究人员对定制微凝胶开展了mRNA-seq分析,以揭示其指导MSC命运的机制。在成软骨诱导7天后,研究人员比较了在对照微凝胶和CH-微凝胶中生长的MSC,总共发现了4408个差异表达基因(DEG)。为了更好地了解参与软骨再生的DEG的基因功能,再将其分为软骨细胞调节和免疫调控。结果显示,与软骨细胞增殖相关的基因显著上调,而与免疫反应相关的基因则下调,包括对IL-1的反应、白细胞迁移、炎症反应调节和T细胞介导的免疫等。KEGG富集分析显示,3条通路上调(包括hedgehog、rap1和p53通路),8条与免疫调控和软骨细胞肥大相关的通路下调,表明CH-微凝胶能够促进成软骨分化并抑制炎症。
同样地,在成骨诱导7天后,研究人员比较了在对照微凝胶和OS-微凝胶中生长的MSC。研究人员共分析了2158个下调DEG和3213个上调DEG。GO分析表明上调的基因与成骨细胞分化、骨化、骨发育、骨生长和骨矿化相关。KEGG分析显示,与骨发育相关的通路(包括PI3K-Akt、FoxO、TGF-β、MAPK和Wnt通路)和免疫调控相关通路(mTOR、TNF和IL-17通路)显著上调,而与细胞凋亡相关的p53信号通路则显著下调。这些结果表明,OS-微凝胶能够促进成骨分化并抑制免疫反应。
利用自组装骨软骨类器官来治疗体内骨软骨缺损
之后,研究人员利用比格犬股骨滑车缺损模型,测试了自组装形成的骨软骨类器官在治疗体内骨软骨缺损上的效果。他们将预分化的定制微凝胶依次注入比格犬的骨软骨缺损处,在原位自组装形成骨软骨类器官,并在术后3个月和6个月对所有膝关节进行采集分析(图3)。术后6个月,对照组的比格犬明显跛行,但微凝胶治疗组的比格犬在步态上明显改善,仅有轻微跛行。核磁共振图像显示,术后3个月和6个月时都存在修复组织(如红色箭头所示)。
在术后3个月,观察骨软骨缺损处的修复组织,发现未治疗对照组和对照微凝胶组几乎没有软骨样组织生长,对于骨软骨类器官组,缺损修复的情况要好得多,但新生组织的外观和平整度仍不如正常软骨。术后6个月,对照微凝胶组的大部分缺损已被填充,但修复组织的外观不平整。而在骨软骨类器官组中,新生组织表现出闪亮且光滑的表面,与周围的软骨很好地整合,没有明显的边界。组织学评估的结果也表明,骨软骨类器官组的缺损再生效果优于其他两组。
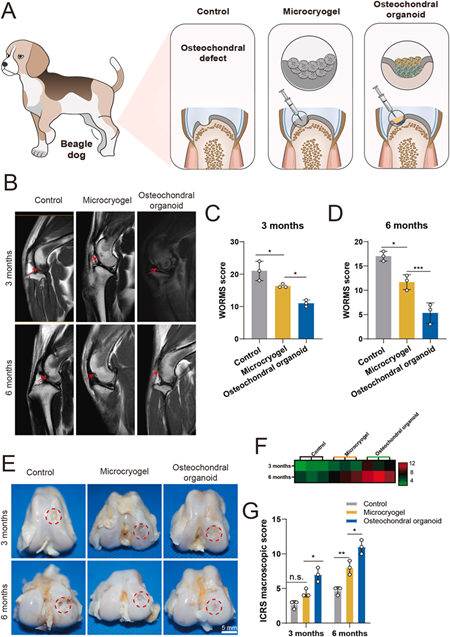
对原位自组装类器官的骨软骨再生进行体内分析[1]
03 研究结论
研究人员此次开发出一种新方法,通过设计定制的微凝胶来分别指导MSC命运,从而构建骨软骨类器官。这些定制的微凝胶显示出良好的细胞相容性以及诱导MSC分化成软骨细胞和骨细胞的强大能力。在体内依次注射定制的微凝胶,可在原位自组装形成骨软骨类器官,实现软骨和软骨下骨的同时再生。这种策略有望实现界面组织的有效再生,而无需采用复杂或严苛的制造工艺。
OriCell®科研MSC及配套培养基
赛业OriCell®作为一家享誉业内的专业细胞产品试剂供应商,可提供骨髓、脂肪、脐带、脐血、牙髓等多种组织来源的间充质干细胞,而且为各种间充质干细胞定制了专门的培养体系,包括完全培养基/无外泌体培养基/无血清培养基,可最大程度维持间充质干细胞的增殖能力并保持分化潜能,而诱导分化试剂盒则可用于间充质干细胞成骨、成脂、成肝和成软骨的定向分化。
| 产品名称 | 货号 |
|
OriCell®人脐带间充质干细胞成骨诱导分化试剂盒 |
HUXUC-90021 |
|
OriCell®人脐带间充质干细胞成软骨诱导分化试剂盒 |
HUXUC-90041 |
填写需求描述给我们
工具快速咨询
400-680-8038
info@oricellbio.cn



