牙髓干细胞是什么?骨髓炎、牙周炎、类风湿关节炎等常见病治疗研究
当牙周炎、类风湿关节炎等炎症性疾病发生时,巨噬细胞被募集并极化为M1促炎表型。这些长期活动的M1巨噬细胞随后产生高水平的NO、活性氧和促炎细胞因子,导致持续的炎症反应。促炎细胞因子可促进成骨细胞产生RANKL的受体激活剂,导致破骨细胞过度形成,从而破坏骨稳态。
间充质干细胞(MSCs)因具有强大的免疫调节能力而被广泛用于各种炎症性疾病的治疗,包括牙周炎。越来越多的证据表明,MSCs的治疗效果主要归因于其分泌的旁分泌因子,其中最关键的是细胞外囊泡(EV),包括外泌体(EXO)、小细胞外囊泡(sEV)。有研究表明,MSC-sEV在免疫调节和诱导组织修复再生等治疗效果上与MSC类似,且在安全性、存储和给药方面比MSC疗法更具优势,因此被认为是一种大有潜力的治疗方法。
牙髓干细胞(DPSCs)是从成人牙髓中分离出来的一种间充质干细胞,其容易获得,且不会引起任何伦理问题。据报道,牙髓干细胞来源小细胞外囊泡(DPSC-sEV)显示出比骨髓间充质干细胞来源小细胞外囊泡(BMSC-sEV)更强的免疫调节作用。不过,DPSC-sEV能否直接抑制巨噬细胞的炎症反应和破骨细胞的生成,目前还是一个未知数。此外,体外培养的MSCs通常暴露在常氧(21% O2)条件下,而体内相当一部分MSCs存在于低氧环境中(2%-8%),那么在低氧条件下产生的DPSC-sEV是否能发挥更好的治疗效果?
为此,中山大学附属口腔医院的研究团队发现,低氧诱导的DPSC-sEV通过调节巨噬细胞极化和破骨细胞生成来改善炎症性骨溶解。这项成果于近日发表在《Bioactive Materials》杂志上,有望为骨髓炎、牙周炎、类风湿关节炎等常见病的治疗带来一种新策略。
研究材料与方法
研究人员从SD大鼠上颌中切牙的牙髓中分离出DPSCs,并鉴定了DPSCs的成骨分化和成脂分化能力(OriCell®MSC成脂诱导分化试剂盒、OriCell®茜素红染色液、OriCell®油红O染色液等产品为该项研究助力)。
之后,研究人员从DPSCs中分离出小细胞外囊泡(sEV),并开展了一系列的分析。在体内研究中,使用了LPS诱导的小鼠颅骨炎性骨吸收模型,体外研究则使用了RAW264.7巨噬细胞。
从DPSCs中分离出sEV,发现低氧诱导了DPSCs的sEV释放
Hypo-sEV诱导巨噬细胞M2极化并抑制破骨细胞生成,从而改善了LPS诱导的炎症性骨吸收
通过miRNA表达谱分析等实验,发现Hypo-sEV的治疗效果是由miR-210-3p介导的
miR-210-3p通过抑制NF-κB1 p105表达,来调节巨噬细胞的炎症反应和破骨细胞的形成
在分离出DPSCs后,研究人员经过流式分析和免疫荧光分析,确认培养的DPSCs具有MSC的间质表型,并具备多潜能分化能力。随后,他们通过超速离心法从常氧(normoxic conditions)和低氧(hypoxic conditions)条件下培养的DPSCs上清液中分离出sEV,分别命名为Nor-sEV和Hypo-sEV。结果发现,这两种sEV都表现出典型的EV特征,但Hypo-sEV的浓度更高,且蛋白质浓度也明显更高。而且,通过sEV蛋白标志物分析,发现低氧明显增加诱导了DPSCs释放sEV。
为了比较这两种sEV对炎症性骨溶解的治疗效果,研究人员使用了LPS诱导的小鼠炎症性骨吸收模型。通过micro-CT扫描和组织学检查评估,他们发现Nor-sEV对LPS诱导的骨溶解未能表现出明显的治疗效果。相反,Hypo-sEV挽救了小鼠颅骨基质的炎症性骨溶解,即提高了BV/TV值,并减少了骨侵蚀面积(图1)。这些结果表明,Hypo-sEV明显改善了LPS诱导的体内炎症性骨吸收。
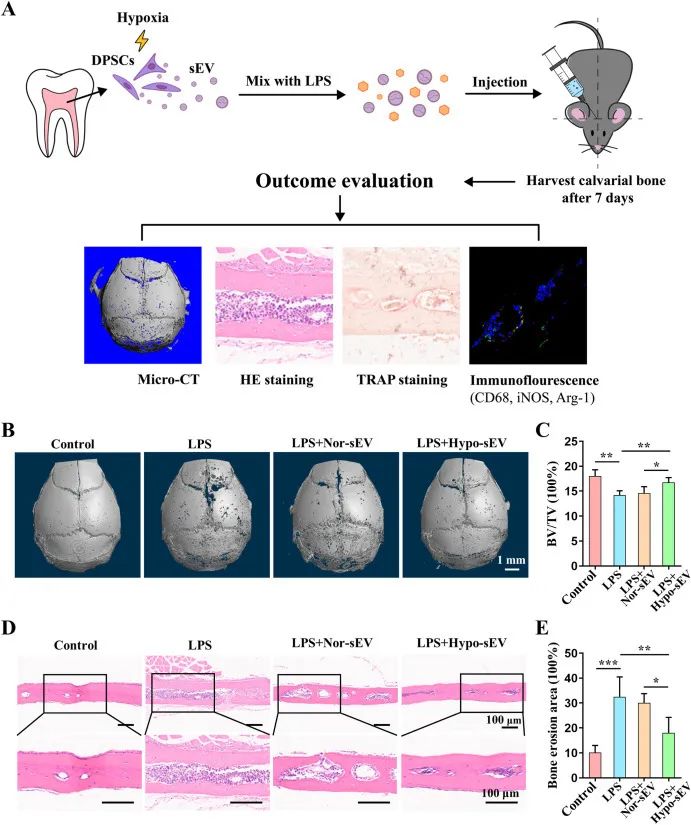
Hypo-sEV在体内抑制LPS诱导的炎症性骨吸收[1]
由于巨噬细胞从M1到M2的表型转变可促进骨修复,故研究人员接着分析了Hypo-sEV是否可促进体内的巨噬细胞M2极化。LPS导致CD68+iNOS+巨噬细胞(M1表型)数量增加,但Hypo-sEV和Nor-sEV的加入使得颅骨基质中出现了更多的CD68+Arg1+巨噬细胞(M2表型),且Hypo-sEV处理后的M1巨噬细胞更少,M2巨噬细胞更多。与Nor-sEV相比,Hypo-sEV明显抑制IL-1β的表达,促进IL-10和Arg1的表达。由此可见,Hypo-sEV可以抑制LPS诱导的巨噬细胞炎症反应,并诱导巨噬细胞M2极化。
炎症性骨吸收是由破骨细胞的过度生成引起的,因此研究人员还研究了Hypo-sEV是否能抑制体内破骨细胞的生成。他们发现,Nor-sEV和Hypo-sEV都减少了LPS诱导的破骨细胞(TRAP阳性)数量,且Hypo-sEV组的破骨细胞数量低于Nor-sEV组。体外培养实验也表明,这两种sEV抑制了RANKL诱导的破骨细胞分化,且Hypo-sEV组的抑制效果优于Nor-sEV组。这些数据显示,Hypo-sEV在体内和体外直接抑制了破骨细胞生成。
为了进一步分析这背后的分子机制,研究人员决定从miRNA研究入手。他们利用新一代测序分析了Nor-sEV和Hypo-sEV的miRNA表达谱。结果发现,与Nor-sEV相比,Hypo-sEV中有45个miRNA上调,64个miRNA下调。在重点关注与巨噬细胞炎症反应或破骨细胞分化有关的miRNA后,他们还发现Hypo-sEV中的miR-7578、miR-187-3p和miR-210-3p水平相对于Nor-sEV升高。后续分析显示,miR-210-3p在介导Hypo-sEV的治疗效果方面发挥了关键作用。
接着,通过对RAW264.7细胞与两种sEV的共培养分析,进一步发现了Hypo-sEV可以将miR-210-3p递送到巨噬细胞和破骨细胞中。miR-210-3p抑制剂提高了促炎细胞因子和iNOS的表达,同时降低了IL-10和Arg1的表达,减弱了Hypo-sEV诱导巨噬细胞M2极化的能力。此外,miR-210-3p抑制剂也部分降低了Hypo-sEV抑制破骨细胞形成的能力以及破骨细胞生成相关基因的表达(图2)。这些结果表明,Hypo-sEV通过上调miR-210-3p表达而诱导巨噬细胞M2极化并抑制破骨细胞生成。
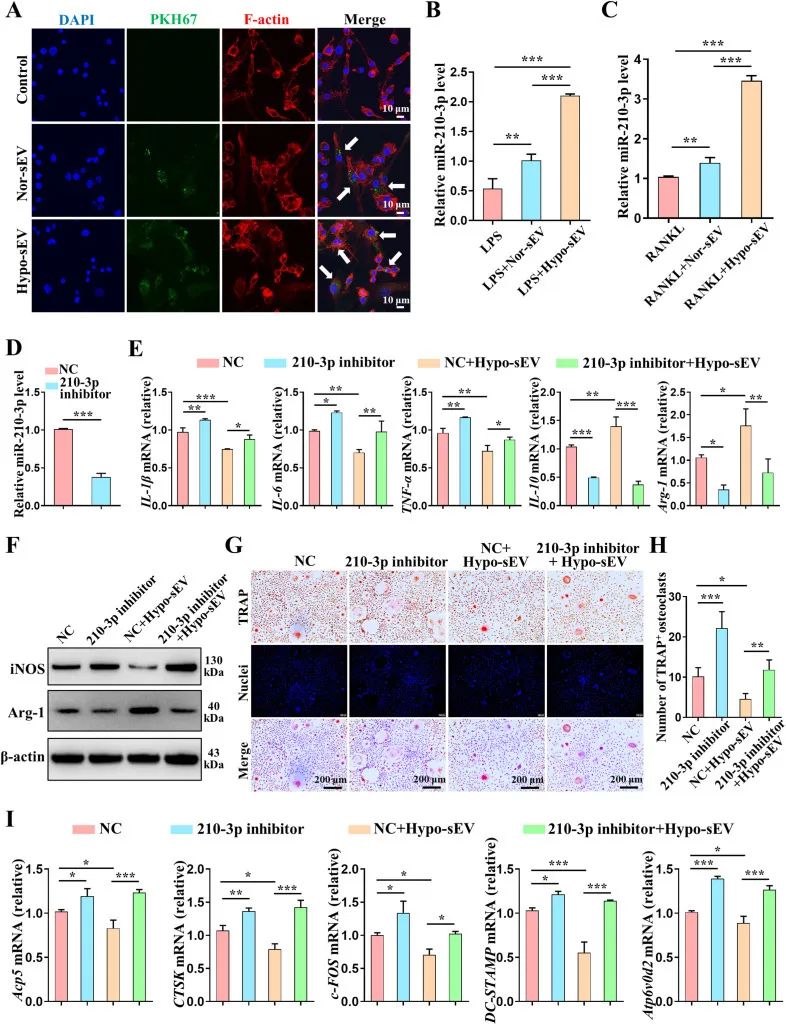
Hypo-sEV在体外通过递送miR-210-3p而诱导巨噬细胞M2极化并抑制破骨细胞生成[1]
之后,实验转移到小鼠模型上继续进行。为了进一步确认Hypo-sEV的治疗效果是由miR-210-3p介导的,研究人员在LPS诱导的炎症性骨吸收模型中使用了miRNA抑制剂antagomir-210-3p。结果显示,antagomir-210-3p明显消除了Hypo-sEV的治疗作用。而且与对照相比,antagomir-210-3p的加入导致M1型巨噬细胞增加,M2型巨噬细胞减少。这些结果证实。miR-210-3p通过诱导巨噬细胞M2极化和抑制破骨细胞生成而明显改善了LPS诱导的炎症性骨溶解。
后续的分析发现,miR-210-3p直接靶向了NF-κB1的3′UTR,而NF-κB通路的激活对巨噬细胞M1极化和破骨细胞生成至关重要。miR-210-3p通过抑制NF-κB1 p105表达来调节巨噬细胞的炎症反应和破骨细胞的形成。
结论
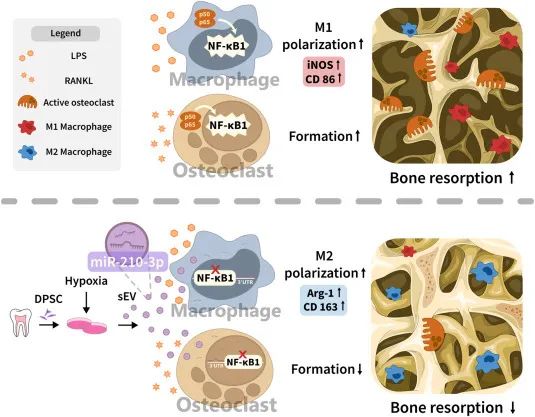
miR-210-3p抑制LPS诱导的炎症性骨吸收的示意图[1]
这项研究表明,低氧预处理不仅诱导了DPSC-sEV的分泌,还增强了DPSC-sEV介导的对LPS诱导的骨溶解的治疗效果。其中,miR-210-3p通过诱导巨噬细胞M2极化和抑制破骨细胞生成来保护骨骼。
因此,低氧诱导的DPSC-sEV和miR-210-3p的这种“一石二鸟”作用有助于开发新策略来治疗炎症性或感染性骨溶解。
原文检索
[1]Jun Tian, Weiyang Chen, Yuhua Xiong, et al. Small extracellular vesicles derived from hypoxic preconditioned dental pulp stem cells ameliorate inflammatory osteolysis by modulating macrophage polarization and osteoclastogenesis. Bioactive Materials, Volume 22, 2023, Pages 326-342, ISSN 2452-199X. https://doi.org/10.1016/j.bioactmat.2022.10.001.
填写需求描述给我们
工具快速咨询
400-680-8038
info@oricellbio.cn



