国家纳米科学中心研究团队设计双面干细胞贴片促进牙周组织再生
牙周治疗的最终目的是将牙周韧带穿梭衔接新生的牙槽骨和牙骨质之间,这种复杂的软硬组织结构需要时间空间层面的有序修复,先后包括牙根表面的牙骨质的形成、牙周韧带的附着以及牙槽骨缺损的修复。如果牙龈上皮率先附着根面,会形成牙周袋,牙槽骨附着根面将形成根骨粘连,从而阻止了牙周组织的完全再生。牙周创面的无血管根面增加了修复的难度,同时局部的炎症环境会对内源性干细胞的增殖与成牙分化能力造成损伤,增加了自身修复的难度。

对此,国家纳米科学中心研究团队结合牙周组织结构特征,设计相匹配的生物支架材料封装干细胞,促进局部牙周组织再生。这篇题为“Stem cell Janus patch for periodontal regeneration”的文章于今年发表在《Nano Today》杂志上(IF = 20.722)。
研究材料
牙龈上皮细胞;牙髓间充质干细胞(DPSC);牙髓间充质干细胞成骨诱导分化试剂盒(由赛业OriCell®提供,产品升级后为:OriCell®人相关干细胞成骨诱导分化试剂盒,货号HUXXC-90021);
小鼠、大鼠和猪的牙周骨缺损模型等.......
研究思路与路线
这项研究设计了一种负载干细胞的双面贴片(Stem cell Janus patch,SCJP),旨在为干细胞构建充分的成骨成牙微环境,同时促进干细胞的旁分泌作用,从而全面促进牙周再生。其阻隔层则通过致密的物理屏障阻隔牙龈上皮细胞的入侵形成牙周袋(图1)。
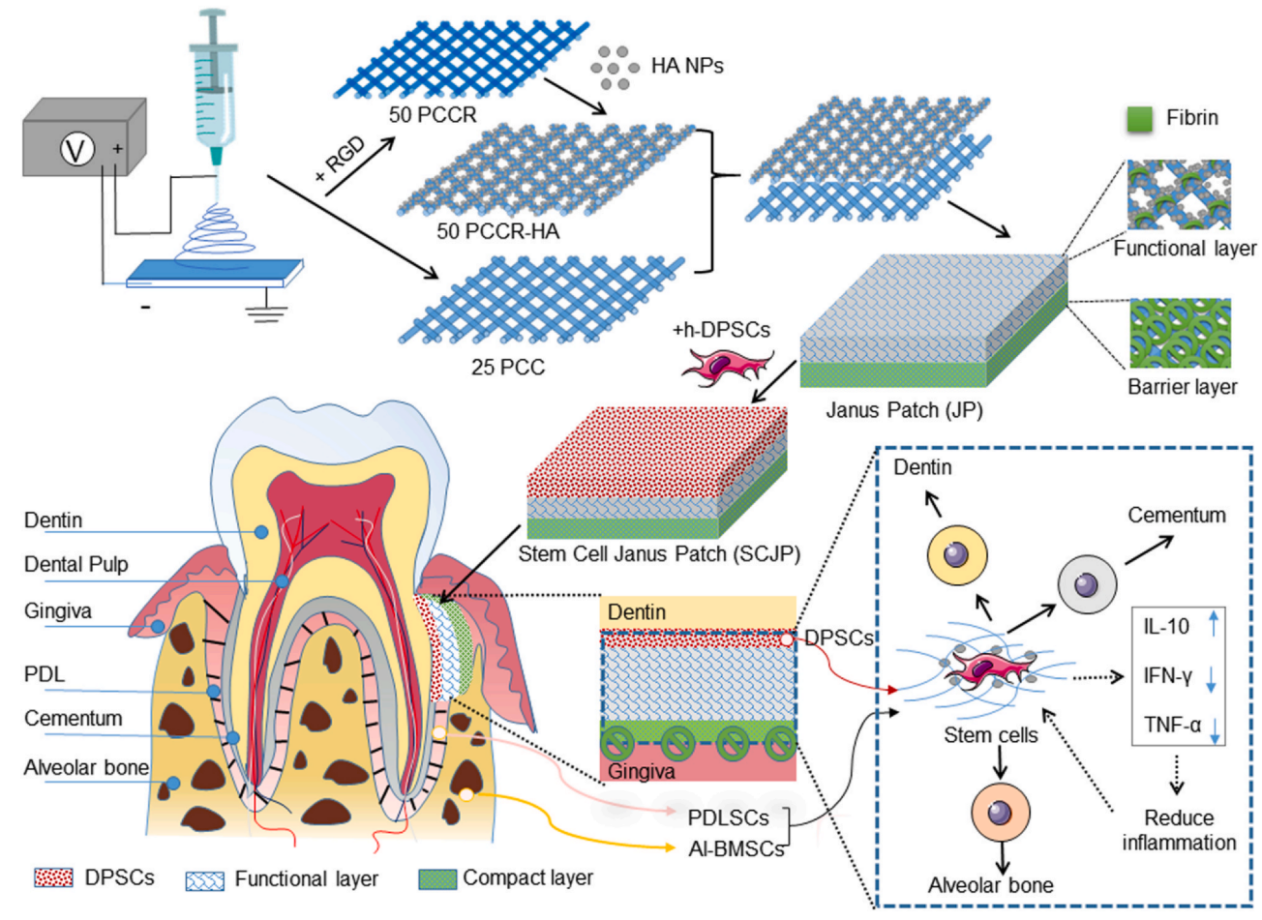
图1. 实验设计原理
实验结果
功能层促进细胞成骨成牙分化
随着n-HA(羟基磷灰石纳米颗粒)悬浮液浓度的增加,沉积附着在纤维上的HA颗粒数量逐渐增加。当n-HA的沉积浓度在1mg/ml的浓度时,纳米颗粒在纤维表面分布密度达到最大,而更高的浓度(> 1mg/ml)会导致纳米颗粒的结块和不均匀的分散。因为n-HA在纤维表面沉积会为细胞提供更多的附着位点,细胞处理4小时后的F-actin染色结果显示,1mg/ml浓度下的n-HA浓度更有利于细胞的粘附和形态铺展。
研究团队对在HA@50PCCR上的细胞的基因水平进行统计分析,发现随着HA颗粒的附着程度的增加,细胞成牙(DSPP、CEMP-1)和成骨基因(RUNX-2)的表达也升高。研究团队最终选择1.0HA@50PCCR作为功能层,促进细胞粘附铺展的同时促进细胞成牙和成骨分化,从而促进牙周组织再生(图2)。
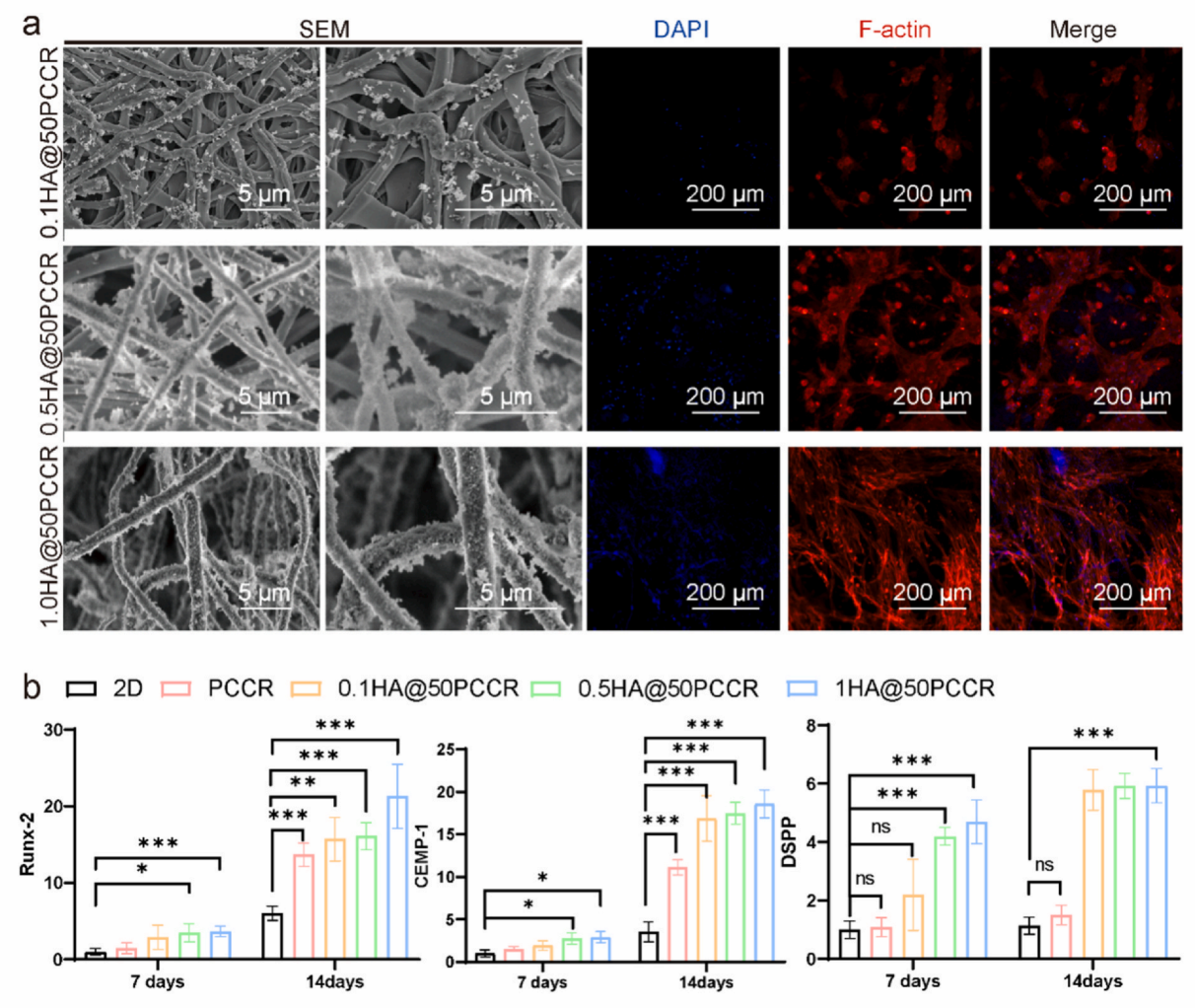
图2. 不同条件HA@PCCR对成牙分化的影响探究
阻隔层的阻止上皮细胞入侵
25PCC具有更小的纤维直径,从而具有更低的孔隙率,更强的阻隔性能。同时25PCC对细胞的粘附能力也较差,因此我们选择25PCC作为阻隔层的修饰材料。随着纤维蛋白原的浓度增加,F@25PCC表面的孔隙率也逐渐降低,有助于阻隔上皮细胞入侵。我们对孔径最小的9F@25PCC进行相关阻隔性能的实验,其在长达4周的时间里表现出良好的阻隔牙龈上皮细胞(GECs)的能力(图3)。

图3. 不同条件下F@PCC对上皮细胞的阻隔能力探究
SCJP促进大鼠牙周组织再生
当SCJP材料原位贴于根部表面时,靠近牙根部的细胞会在根面矿化,并有能力分化出牙本质和牙骨质来修复根部表面的损伤,从而促进牙周膜的新的附着。同时,牙槽骨一侧的干细胞能进行成骨分化,从而促进牙槽骨修复。为了确定SCJP在体内的再生能力,研究团队将贴片植入大鼠的牙周缺损处,并与大鼠牙周缺损处无支架移植组的阴性对照组以及拥有健康牙周的大鼠(sham group)进行比较。

图4. 双面干细胞贴片原位促进牙周组织再生
结论
实验结果表明,功能层镶嵌羟基磷灰石纳米颗粒,同时负载牙髓间充质干细胞,高效促进了牙本质、牙骨质和牙槽骨的再生,从而进一步实现了完整的牙周组织再生。另一侧的阻隔层凭借致密的结构和增强的机械性能,有效地防止上皮细胞的入侵。在小鼠、大鼠和猪的牙周骨缺损模型中,双面干细胞贴片分别实现了成功的异位矿化与进一步的成骨成牙分化的能力,从而验证了该贴片在诱导牙周组织再生方面的潜力。这项工作提出了一种安全和有效的干细胞组织工程治疗策略,为中重度牙周炎的全面牙周组织再生提出了一种可行的方案。
原文检索:
Na Yan, Bin Hu, Junchao Xu, Rong Cai, Zhenhai Liu, Dapeng Fu, Beibei Huo, Zhenhua Liu, Yuliang Zhao, Chunying Chen, Weihua Xu. Stem cell Janus patch for periodontal regeneration, Nano Today, Volume,42,2022,
赛业OriCell®干细胞诱导分化
依赖于成熟的干细胞技术平台,我们可以为您开展多种干细胞分化潜能研究的实验服务。其中针对特定种属优化定制的诱导分化试剂盒,可向成骨、成脂、成软骨、成肝等多个方向诱导,性能稳定,诱导分化效果好!同时,我们可以按照您提供的诱导试剂和诱导方法为您完成特定的干细胞诱导实验,也可以按照您的目的和要求,在各种干细胞诱导途径中为您探索出一套相对完善的方法。
活动推荐
现牙髓干细胞及相关培养基参与夏日大促中,还可享赠多种豪礼,欢迎联系咨询。
填写需求描述给我们
工具快速咨询
400-680-8038
info@oricellbio.cn




