Chem. Eng. J | 同济大学附属妇产科医院团队开发负载维立西呱可注射水凝胶,为宫腔粘连治疗提供新策略
在妇产科领域,宫腔粘连(IUA)引发的子宫性不孕是一大难题,严重困扰着众多患者。IUA主要由刮宫、剖宫产、肌瘤切除术等手术创伤导致子宫内膜纤维化瘢痕形成。患者常面临闭经、不孕、反复流产以及胎盘植入异常等问题,其中不孕和流产对育龄女性的影响尤为严重。据统计,全球范围内IUA的发病率呈上升趋势,成为导致女性不孕的重要原因之一。目前,针对IUA不孕的治疗手段有限。宫腔镜手术是IUA手术治疗的基石,包括用剪刀进行粘连分解、对更广泛粘连采用电灼和激光消融等技术。然而,这些手术存在显著局限性,如术后再粘连风险高,对于严重的IUA病例治疗效果不佳。辅助治疗方法,如口服雌激素或宫腔内球囊扩张,与宫腔镜粘连分解术联合使用时,也无法将受损的子宫内膜完全修复至利于妊娠的状态。因此,寻找更有效的治疗方法迫在眉睫。
近日,同济大学附属妇产科医院等机构学者利用细胞模型和动物模型探究了一氧化氮(NO)信号缺乏参与宫腔粘连的发病机制,并且针对此机制提出利用NO受体刺激剂治疗宫腔粘连的可能性。这项研究成果发表在《Chemical Engineering Journal》期刊上(IF 13.4)。

文献封面截图[1]
研究材料与方法
本项研究主要应用了非靶向代谢组学测序,免疫组织化学,Western Blot,肌成纤维细胞模型的构建,宫腔粘连大鼠模型的构建。其中细胞模型使用了Ishikawa人子宫内膜癌细胞系,原代人子宫内膜基质细胞模型 (其中细胞培养所用血清为赛业OriCell®特级胎牛血清)。
1. 非靶向代谢组学检测,发现宫腔粘连的子宫内膜存在NO信号缺乏。
2. 细胞实验证明NO受体刺激剂维立西呱有效改善子宫内膜基质细胞纤维化和氧化应激。
3. 为了延长维立西呱在子宫内膜的留置时间,合成一种可注射水凝胶并进行表征。
4. 动物实验验证负载维立西呱可注射水凝胶治疗宫腔粘连的效果和安全性。

研究示意图[1]
利用宫腔粘连SD大鼠模型进行非靶向代谢组学测序,研究团队发现差异代谢物主要聚集在尿素循环中。然而此循环中瓜氨酸、天冬氨酸、精氨琥珀酸和延胡索酸明显在宫腔粘连组降低,其余代谢物均无表达差异(图2)。这暗示差异代谢物更集中在精氨酸-瓜氨酸-精氨琥珀酸循环中。值得注意的是,精氨酸在合成瓜氨酸的同时会产生NO,这是体内NO生物合成的关键代谢通路。因此,宫腔粘连的子宫内膜存在NO信号的缺乏。

大鼠受损子宫内膜的代谢组学测序结果[1]
NO受体刺激剂维立西呱有效抑制肌成纤维细胞的纤维化和氧化应激
考虑到宫腔粘连的子宫内膜存在NO信号缺乏,研究人员在细胞层面探究了NO受体刺激剂维立西呱对肌成纤维细胞的作用。首先,利用TGF-β1处理原代子宫内膜基质细胞诱导形成肌成纤维细胞(其中细胞培养所用胎牛血清由赛业OriCell®提供)。研究发现存在维立西呱的情况下,肌成纤维细胞的标志物COL1A1和α-SMA表达会明显降低,暗示了维立西呱抑制纤维化的潜力(图3)。此外,现存在维立西呱的情况下,细胞产生的ROS水平和线粒体mPTP的开放也都被明显抑制,暗示了暗示了维立西呱抑制氧化应激的潜力(图3)。细胞实验最终发现维立西呱通过激活sGC/cGMP/SMAD7信号通路,促进SMAD7表达,抑制SMAD3磷酸化,从而发挥抗纤维化和抗氧化应激作用。

维立西呱对TGF-β1诱导的肌成纤维细胞分化、ROS积累和mPTP开放的抑制作用[1]
可注射水凝胶的表征
研究人员开发了基于氧化透明质酸(HA-CHO)和酰肼接枝透明质酸(HA-ADH)的可注射载药水凝胶。对水凝胶的特性进行全面表征,包括其微观结构、溶胀性、降解性、流变学特性以及药物释放性能等(图4)。考虑到4%的水凝胶的膨胀性和降解性优于2%水凝胶,后续研究利用4%的水凝胶负载维立西呱。结果显示水凝胶可以逐步释放维立西呱,并且在体内大约20天会降解(图4)。
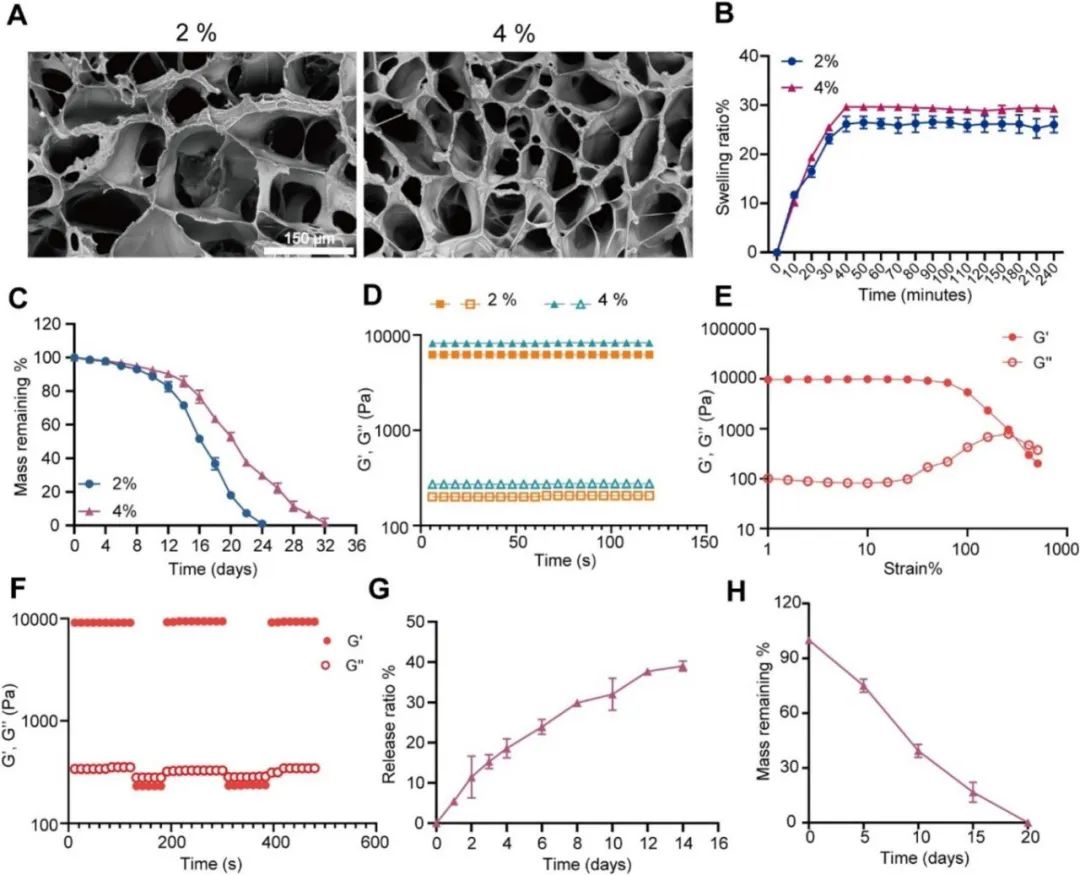
可注射水凝胶的表征[1]
负载维立西呱的可注射水凝胶有效修复了受损的子宫内膜
为了探究负载维立西呱的可注射水凝胶对宫腔粘连的治疗,研究团队利用机械损伤构建了宫腔粘连的SD大鼠模型。将其随机分配到了不治疗组,口服维立西呱治疗组,局部维立西呱治理组,局部水凝胶治疗组和局部负载维立西呱水凝胶治疗组。研究最终发现各个治疗组均不同程度修复了受损的子宫内膜,并且局部负载维立西呱水凝胶治疗效果最佳。负载维立西呱显著增加了子宫内膜的厚度,血管数量,并且促进了抗纤维化的SMAD7表达,抑制了诱导氧化应激的NOX4的表达。
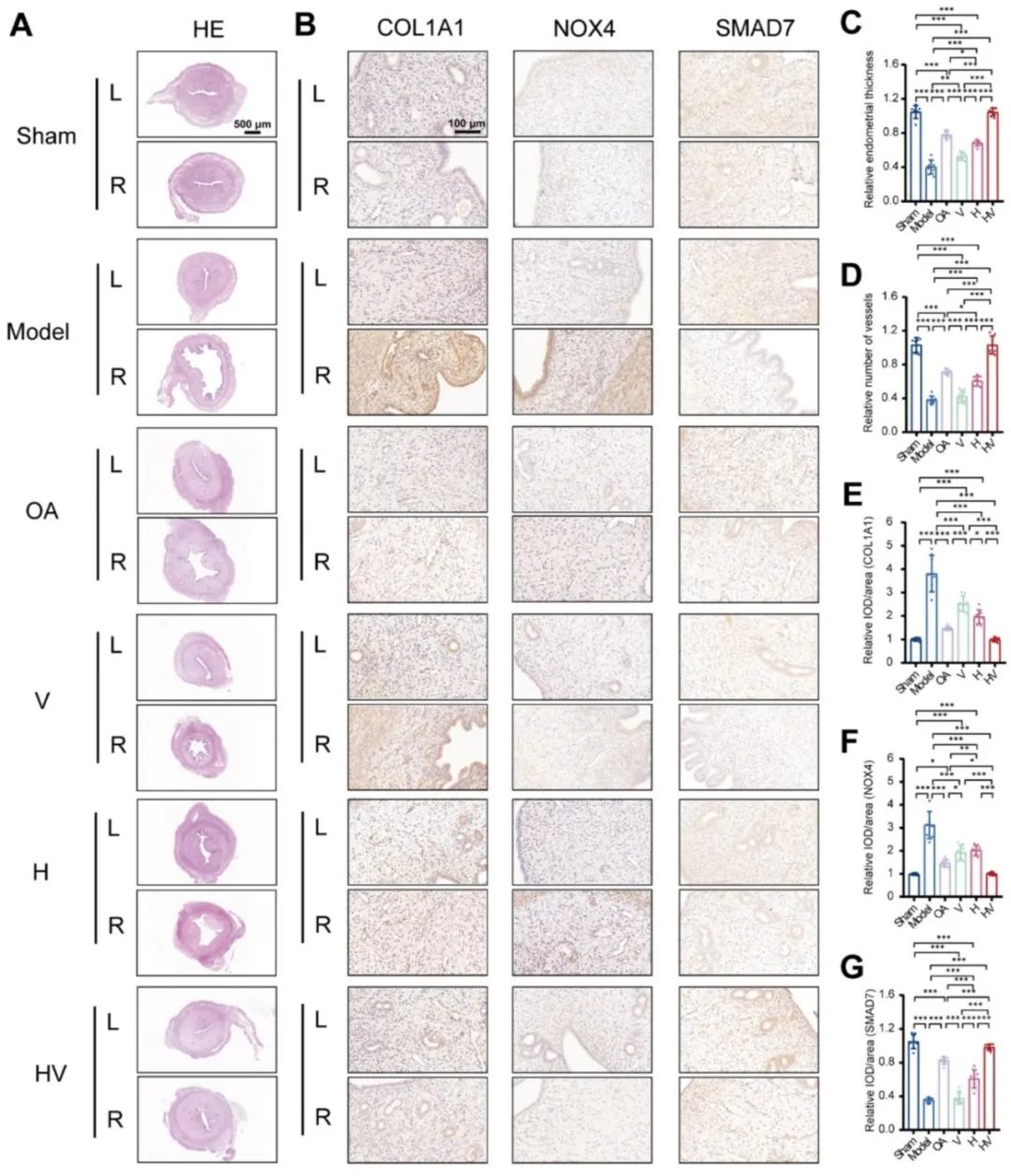
负载维立西呱的可注射水凝胶有效修复了受损的子宫内膜[1]
IUA常由手术创伤致使子宫内膜纤维化,患者多面临不孕、流产等困扰,现有治疗手段效果不佳。研究发现,IUA患者子宫内膜NO信号受损。而维立西呱作为NO受体刺激剂,具有潜在的抗纤维化作用。为验证这一设想,研究团队构建大鼠子宫内膜损伤模型,并进行多方面实验。
-
体外实验结果显示,维立西呱可抑制TGF-β1诱导的子宫内膜间质细胞向肌成纤维细胞分化,降低NOX4表达和ROS积累,其机制是通过激sGC/cGMP/SMAD7信号通路,抑制SMAD3磷酸化。为增强维立西呱疗效,研究团队制备了基于氧化透明质酸和酰肼接枝透明质酸的可注射载药水凝胶,该水凝胶具备良好的生物相容性、可注射性和缓释性能。
-
动物实验结果显示,水凝胶和维立西呱联合治疗能有效修复受损子宫内膜,增加内膜厚度,促进血管生成,显著降低纤维化程度。口服维立西呱和单纯水凝胶治疗也有一定修复效果,但联合治疗效果最佳。
综上所述,负载维立西呱的水凝胶为IUA治疗提供了新方向,有望改善患者生育状况,也为其他纤维化疾病治疗提供了新思路。
原文检索:
[1] Antifibrotic and antioxidant injectable hydrogel boosts endometrial repair and fertility via sGC/cGMP/SMAD7 signaling activation, Chemical Engineering Journal, (2025) https://doi.org/10.1016/j.cej.2025.162672.
填写需求描述给我们
工具快速咨询
400-680-8038
info@oricellbio.cn



