Research:一种干细胞招募和骨诱导功能的新型仿生肽用于改善骨愈合
随着骨质疏松症的发病率逐年增高,植骨手术的治疗效果正面临严重的挑战。钛合金是最受欢迎的骨科植入材料之一,但由于缺乏生物活性,钛基材料的表面不利于细胞粘附和生长,特别是成骨细胞。此外,骨质疏松症患者的骨髓微环境发生改变,也会延缓骨修复和再生。因此,需要更好的策略来促进骨整合。
因此,苏州大学附属第一医院和江苏大学领导的研究团队开发出一种新策略,通过两种生物活性肽来诱导骨再生,并显著改善骨质疏松症患者的植骨效果。这项研究成果于9月发表在《Research》杂志上。

研究材料与方法
研究人员建立了老年性骨质疏松症大鼠模型,并分离出骨质疏松BMSC(op-BMSC)用于后续分析。然后,分别通过transwell迁移分析以及碱性磷酸酶和茜素红S染色来评估BMSC招募和成骨分化(期间使用了由赛业OriCell®提供的骨髓间充质干细胞成骨诱导分化试剂盒)。最后,采用了Micro-CT分析,评估植入物的骨整合能力。
技术路线
1. 采用生物活性肽DOPA-E7和DOPA-Y5对钛基植入物进行修饰。
2. 评估仿生涂层的生物相容性,并在体外评估涂层对BMSC招募、定植和成骨分化的影响。
3. 探索op-BMSC与肽涂层相互作用的分子机制。
4. 以老年性骨质疏松症大鼠为模型,评估仿生涂层对体内BMSC招募和骨整合的影响。
研究结果
钛基材料的表面改性
研究人员受到贻贝足粘蛋白的启发,采用两种生物活性肽(DOPA-E7和DOPA-Y5)来修饰钛种植体的生物活性(图1)。其中,EPLQLKM(E7)能够促进干细胞的粘附和增殖;YGFGG(Y5)则来源于成骨生长肽,能够调节成骨分化。在成功合成两种多肽后,他们对钛基材料的表面进行了包被,制备出DOPA-E7和DOPA-Y5多肽修饰表面。他们发现,这些生物活性肽能够固定在钛基材料的表面上。
同时,研究人员还建立了老年性骨质疏松症大鼠模型(18月龄的雄性大鼠)。与正常对照组(3月龄的雄性大鼠)相比,骨质疏松组的骨密度、骨体积分数和骨小梁厚度都显著降低。他们从这些大鼠中分离出骨髓间充质干细胞(op-BMSC),并发现这些细胞的增殖、迁移和成骨能力显著减弱。这说明需要通过修饰骨种植体,为BMSC的增殖、趋化和成骨分化创造良好的环境。
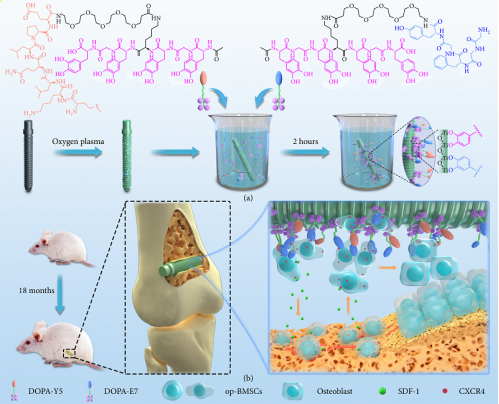
图1. 研究示意图[1]
体外op-BMSC招募和成骨分析
研究人员首先评估了涂层材料的生物相容性。与裸钛组相比,包被不同摩尔比的两种仿生肽后,死细胞数量明显减少,且op-BMSC表现出明显的增殖和存活能力。材料表面经过活性肽修饰后,op-BMSC能够更好地粘附,并增加了丝状F-肌动蛋白的表达。这些结果表明,这两种仿生肽修饰的表面对op-BMSC的粘附和增殖有积极的影响。
原位骨形成需要BMSC的招募、定植和成骨分化。因此,他们首先评估了不同比例的表面对op-BMSC的迁移诱导作用。transwell迁移分析的结果表明,包含DOPA-E7的涂层都可以诱导更多的op-BMSC迁移(图2)。进一步分析后发现,在DOPA-E7诱导op-BMSC迁移和分化的过程中,趋化因子SDF-1α很可能起了重要作用。同时,包含较多DOPA-E7(即4:0、3:1和2:2)的涂层表现出更强的BMSC捕获能力。

图2. 体外op-BMSC招募[1]
接着,研究人员评估了仿生肽修饰的表面对成骨分化的影响。考虑到衰老环境内的成骨能力减弱,op-BMSC更倾向于在缺损部位诱导成骨,因此他们采用赛业OriCell®BMSC成骨诱导分化试剂盒进行体外分化。碱性磷酸酶(ALP,成骨分化标志物)的染色结果表明,DOPA-Y5较高的组表现出明显更深的蓝色。在成骨诱导4天后,他们还分析了多个蛋白的表达,包括关键调节因子Runx2,发现三个组(即4:0、3:1和2:2)的荧光强度显著高于其他组。这些结果显示,包含DOPA-Y5的肽涂层增强了BMSC的体外成骨能力。
在对这些体外分析结果进行全面评估后,研究人员认为以2:2的DOPA-E7/DOPA-Y5比例包被钛基材料表面效果最好。它能够有效捕获干细胞,并促进干细胞粘附、增殖和成骨分化。因此,后续实验采用2:2的比例对医用钛螺钉表面进行功能修饰。
为了确定op-BMSC与肽涂层相互作用的分子机制,通过RNA测序比较了包被前后的基因表达谱。结果表明,DOPA-E7肽涂层可能通过调节CXCR4-CXCL12趋化因子信号通路来促进op-BMSC迁移。具体机制是,DOPA-E7与BMSC表面的CXCR4受体结合后,促进细胞自分泌SDF-1α,而分泌出的SDF-1α又可以与其他干细胞表面的CXCR4受体结合,形成化学级联反应,从而不断招募内源性干细胞。
体内细胞招募和骨整合分析
研究人员评估了仿生涂层对体内BMSC招募的影响。他们将钛螺钉植入老年性骨质疏松大鼠的股骨远端,一周后评估骨螺钉界面处的op-BMSC积累。结果发现,与对照组相比,DOPA-E7组和DOPA-(E7+Y5)组的CD146阳性细胞数量显著增加。总的来说,通过DOPA将E7活性肽移植到骨植入材料的表面,然后定向招募BMSC,是骨界面整合的前提条件。
体内植入8周后,他们评估了螺钉和骨组织交界处的骨形成和骨整合。DOPA-(E7+Y5)螺钉组产生了最高的骨体积分数,并表现出最佳的小梁结构(图3)。H&E和Masson染色结果表明,DOPA-(E7+Y5)组的骨-植入物界面有完全融合的骨组织,DOPA-(E7+Y5)大鼠的骨骼成熟度和钙化程度也更高。这些结果表明,DOPA-(E7+Y5)肽涂层植入物可促进老年性骨质疏松大鼠的骨再生和修复。

图3. 仿生肽处理的螺钉在体内增强了成骨分化[1]
结论
总的来说,研究人员设计出两种来源于贻贝的生物活性肽,并对钛基植入物进行生物修饰。这种修饰能够有效提高钛基植入物的生物相容性,并促进内源性BMSC的粘附、定植、增殖和成骨分化。
这项研究还证明,适当比例的仿生肽组合能够显著增强体内骨植入物的骨生成和骨整合。它为实现有效的原位骨再生和改善医学植入物的临床结果提供了一种安全可行的策略。
原文检索:
[1]Bai J, Ge G, Wang Q, Li W, Zheng K, Xu Y, Yang H, Pan G, Geng D. Engineering Stem Cell Recruitment and Osteoinduction via Bioadhesive Molecular Mimics to Improve Osteoporotic Bone-Implant Integration. Research (Wash D C). 2022 Sep 6;2022:9823784. doi: 10.34133/2022/9823784.
填写需求描述给我们
工具快速咨询
400-680-8038
info@oricellbio.cn



